Обзорная статья за авторством AHMET TEZEL & CLENN H. FREDRICKON, Калифорнийский университет, Санта-Барбара, США
Абстракт
Введение: Использование инъекционных препаратов в контурной пластике мягких тканей в США на фоне появления новых дермальных филлеров, содержащих гиалуроновую кислоту (ГК), становится все более распространенным. Дермальные филеры на основе ГК значительно отличаются друг от друга по физическим и химическим свойствам, и на их окончательные клинические характеристики влияют многие факторы. В статье рассматриваются общие научные представления о свойствах ГК и описывается, как физические характеристики дермальных филлеров, содержащих ГК, могут влиять на клинические исходы. Гиалуроновая кислота: описан химический состав дисахаридных мономеров ГК, механизм образования полимерных цепей и их перекрестного связывания с образованием геля, используемого в качестве дермального филлера. Дермальные филлеры на основе гиалуроновой кислоты: представлены определения основных понятий и свойств, связанных с производством дермальных филлеров на основе ГК, которые влияют на их окончательные характеристики, например «степень перекрестного связывания», «твердость геля», «консистенция геля», «вязкость», «сила выдавливания», «концентрация ГК» и «степень гидратации». Новые дермальные филлеры на основе ГК, недавно одобренные Управлением по контролю за продуктами и лекарствами США, отличаются от представленных в настоящее время на рынке препаратов и могут обеспечивать простоту введения и длительное сохранение эффекта, по сравнению с филлерами предыдущего поколения.
Выводы: Знание химических и физических свойств дермальных филлеров, содержащих ГК, поможет врачам выбрать в каждом конкретном случае наиболее подходящий препарат для контурной пластики лица. В сочетании с правильной техникой инъекции и достаточным опытом это поможет достичь тех результатов, которыми будут довольны пациенты.
Ключевые слова: дермальные филлеры, гиалуроновая кислота, контурная пластика
Введение
С возрастом на наших лицах начинают появляться следы от действия силы земного притяжения, солнечных лучей и многолетних мимических движений: улыбок, жевания, прищуривания. Нижерасположенные мягкие ткани, которые позволяют нашей коже выглядеть молодой, начинают разрушаться и появляются морщины вокруг глаз, глубокие носогубные сладки и морщины-заломы. Вводимые в мягкие ткани филлеры способны заполнить эти морщины и складки, на время делая лицо более гладким и помолодевшим [1]. Идеальный филлер не должен быть постоянным (перманентным), однако необходимо, чтобы эффект от его действия сохранялся в течение длительного времени, а сам препарат вызывал минимальные побочные эффекты, не требовал постановки аллергических проб, был простым в применении/введении, безболезненным при инъекции, а также экономически эффективным и для врача, и для пациента [2].
На протяжение более чем 20 лет единственными дермальными филерами, разрешенными для применения Управлением по контролю за продуктами и лекарствами США (FDA) являлись препараты на основе коровьего коллагена (Zyderm, Zyplast; Allergan, Санта-Барбара, Калифорния, СШA). Поскольку эти дермальные филлеры содержали коровий коллаген, одним из их главных недостатков была необходимость постановки аллергических проб. Помимо возможных аллергических реакций, существенной слабой стороной лечения была необходимость заставлять пациентов косметологических клиник, зачастую импульсивных потребителей, в течение месяца ожидать результата аллергических проб перед проведением самой процедуры [3]. В феврале 2003 года Управление по контролю за продуктами и лекарствами США одобрило к применению препараты на основе коллагена человеческого происхождения (CosmoDerm, CosmoPlast; Allergan), которые позволили существенно снизить риск аллергических реакций и отказаться от ранее необходимых аллергических проб.
Другой интенсивно изучаемой характеристикой дермальных филлеров была длительность их действия. Попытки найти филлеры, которые бы не требовали постановки аллергических проб и действовали бы по возможности дольше, чем препараты коллагена, привели к созданию веществ на основе гиалуроновой кислоты (ГК). Первый препарат на основе ГК (Restylane; Medicis Aesthetics Holdings Inv., Скоттсдэйл, Аризона, США) был одобрен для применения в США в декабре 2003 года, и вскоре после этого на рынке появились и другие филлеры, содержащие ГК (Hylaform, Hylaform Plus, Captique, Juvederm Ultra, Juvederm Ultra Plus; Inamed Corporation, в настоящее время – Allergan).
ГК обладает свойствами, которые делают ее крайне подходящей для использования в качестве дермального филлера: так, она способна связывать большое количество воды, присутствует в коже в естественных условиях и не склонна вызывать нежелательные реакции. Несмотря на эти общие черты, все дермальные филлеры на основе ГК отличаются друг от друга. Они содержат разные молекулы-сшивки (перекрестные связыватели, кросслинкеры), отличаются степенью перекрестного связывания, твердостью геля, вязкостью, силой выдавливания, консистенцией геля, общей концентрацией ГК (количеством ГК в 1 мл конечного продукта) и продолжительностью сохранения в коже. Клинические свойства дермального филлера на основе ГК определяются тем, насколько согласованно эти характеристики дополняют друг друга для того, чтобы конечный продукт сочетал в себе простоту введения, длительность действия и эффективность восполнения утраченного объема.
Для того чтобы практикующим врачам было легче оценивать и сравнивать между собой дермальные филлеры на основе ГК, в данной статье предпринимается попытка разъяснить те химические и физические свойства, которые оказывают наиболее значимое влияние на клинические характеристики продуктов. Более глубокое понимание научных сторон, лежащих в основе дермальных филлеров на основе ГК, и факторов, оказывающих влияние на характеристики конечного продукта, должно облегчить подбор подходящей терапии для все большего числа пациентов, обращающихся за контурной пластикой и процедурами восстановления и омоложения.
Гиалуроновая кислота: химический состав
Гиалуроновая кислота (ГК, также известная как гиалуронан) – полисахарид (а именно, глюкозаминогликан), состоящий из повторяющихся остатков D-глюкуроновой кислоты и D-N-ацетилглюкозамин-дисахарида. Как правило, карбоксильная группа (-COOH) D-глюкуроновой кислоты превращается в ее натриевую соль, и образуется дисахарид, строение которого представлено на рисунке 1.
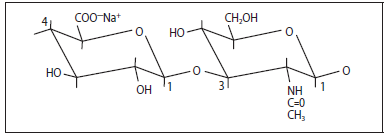
Рисунок 1. Мономер ГК. Один дисахаридный остаток, состоящий из натриевой соли D-глюкуроновой кислоты (слева) и D-N-ацетилглюкозамина (справа), соединенных бета-1,3-гликозидной связью. Обратите внимание, что дисахаридные остатки между собой соединены бета-1,4гликозидной связью.
В более широком смысле эти дисахаридные остатки можно рассматривать как «мономеры» – молекулы с небольшой массой, химически связанные с такими же или другими мономерами в макромолекулу или «полимер». Мономеры дисахарида связаны между собой в линейную цепь полимера ГК бета-1,4-гликозидными связями. Каждый дисахаридный мономер имеет молекулярную массу приблизительно 400 Да. Число дисахаридных повторов (n) в цепи полимера ГК может составлять 25 000 и более, и тогда общая молекулярная масса полимера достигает приблизительно 10 МДа.
Длина цепи и источник происхождения молекулы
ГК – неотъемлемый естественный биополимерный компонент межклеточного вещества всех взрослых животных тканей. Частым заблуждением, касающимся ГК, является представление о том, что ее структура различается в зависимости от источника происхождения: животного или бактериального. Строение основной структурной единицы ГК, то есть мономера, из которого состоит полимерная цепь, одинаковое, вне зависимости от источника происхождения. Главным различием ГК животной и бактериальной природы является длина (степень полимеризации n, или молекулярный вес) конечной цепи полимера. Полимерная цепь ГК бактериального происхождения как правило короче и состоит примерно из 4 000–6 000 мономеров, что соответствует средней молекулярной массе 1,5–2,5 МДа. Цепи ГК животного происхождения состоят из 10 000–15 000 мономеров, что соответствует средней молекулярной массе 4–6 МДа (рисунок 2).
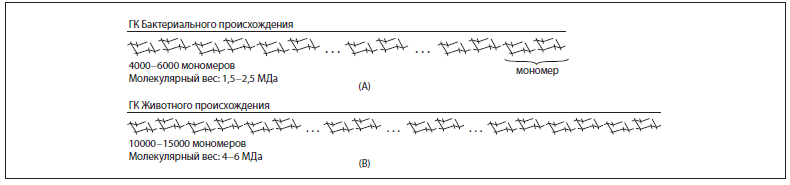
Рисунок 2. Длина цепи ГК. Полимерные цепи ГК состоят из нескольких тысяч дисахаридных мономеров и различаются только длиной цепи, но не основным молекулярным строением. Полимерные цепи ГК бактериального происхождения (А) как правило короче, чем полимерные цепи ГК животного происхождения (B).
(A)ГК бактериального происхождения.4000-6000мономеров. Молекулярнаямасса1,5–2,5 МДа.
(B) ГК животного происхождения. 10000–15000 мономеров. Молекулярная масса 4–6 МДа.
Растворимость в воде
ГК как бактериального, так и животного происхождения – хорошо растворимый в воде полимер, быстро образующий вязкий прозрачный раствор. Растворимость ГК в воде связана с множеством факторов, однако главным образом – с наличием в составе каждого дисахаридного остатка 4 гидроксильных (-OH) и одной «солевой» (–COO-Na+) группы (рисунок 1). Гидроксильная группа способна участвовать в образовании водородных связей с водой, что стабилизирует растворенное состояние. Кроме того, солевая группа в воде диссоциируется с высвобождением свободной энергии, которая возникает из энергии растворения результирующих ионов –СОО- и Na+ и увеличения энтропии высвобождающихся ионов натрия (Na+). В сумме все эти эффекты приводят к тому, что ГК полностью растворяется в воде.
Дермальные филлеры на основе гиалуроновой кислоты
Благодаря тому, что химическая структура ГК одинакова у всех особей, вероятность иммунологических реакций и отторжения имплантата незначительна, и это делает ГК крайне подходящим веществом для использования в качестве дермального филлера [4].
Перекрестное связывание полимеров ГК
Для того чтобы изготовить препарат, который может быть использован в качестве дермального филлера, ГК необходимо подвергнуть ряду химических модификаций и нескольким этапам обработки. Исходный полимер ГК, используемый для производства дермальных филлеров, обычно поставляется изготовителю в виде сухого порошка. При смешивании этого порошка с водой образуется вязкая жидкость, которая по внешнему виду и консистенции напоминает яичный белок. Чем больше порошка ГК добавляется к заданному объему воды, тем более густым и вязким получается раствор (рисунок 3).
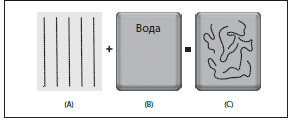
Рисунок 3. Растворение ГК в воде. Полимерные цепи ГК, состоящие из множества мономеров (А) при растворении в воде (В) превращаются в вязкую жидкость (С), которая внешне и по консистенции напоминает яичный белок.
Этот раствор носит название свободной, или перекрестно не связанной, или немодифицированной ГК. Если бы в качестве дермального филлера использовался он, то продукт исчезал бы из точки инъекции очень быстро (менее чем за неделю). Это является следствием очень ограниченного периода сохранения немодифицированной ГК в коже, так как организм крайне быстро разрушает цепи ГК, которые не связаны перекрестно с образованием геля (см. ниже). Ферменты, например гиалуронидаза, и свободные радикалы, в естественных условиях присутствующие в коже, быстро расщепляют перекрестно не связанные полимеры ГК, одномоментно взаимодействуя с большой поверхностью вещества. Как следствие, период полужизни ГК в ткани, где она растворяется в воде, составляет 1–2 дня, после чего осуществляется
ее ферментативное расщепление в печени на воду и диоксид углерода [5]. Таким образом, раствор перекрестно не связанной ГК не сохраняется в точке инъекции, что требуется от дермального филлера [6].
Для того чтобы преодолеть недостаточно длительное сохранение перекрестно не связанной ГК в ткани, производители дермальных филлеров используют молекулысшивки (кросслинкеры). Молекулы-сшивки связывают цепи ГК между собой, создавая полимерную «сеть» и превращая вязкий раствор в гель (рисунок 4).
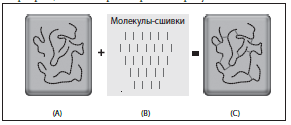
Рисунок 4. Гель ГК. Перекрестное связывание полимерных цепей ГК превращает раствор ГК (A) в гель (С). Молекулы сшивки (В) связывают отдельные полимерные цепи ГК друг c другом в «сеть» (С), которая макроскопически имеет вид гелевой массы.
Это превращение немного напоминает процесс приготовления желатинового десерта. Полученный гель ГК представляет собой единую структуру, которая создает физический и химический барьер для ферментативного и свободнорадикального расщепления. В связи с тем, что полимерный каркас геля содержит множество химических связей, ферменты и свободные радикалы могут одномоментно взаимодействовать лишь с ограниченными по площади участками. Кроме того, в связи с большими размерами полученной структуры, ферменты с трудом проникают в гелевую сеть, что в конечном итоге вносит дополнительный вклад в замедление процесса расщепления. С клинической точки зрения это означает, что гель на основе ГК дольше сохраняется в коже в качестве дермального филлера. Наглядно это можно представить на примере строительного раствора, которым соединяются кирпичи. Подобно тому как строительный раствор делает кирпичную кладку прочнее, молекулы-сшивки повышают стойкость и надежность ГК как биоматериала.
Таким образом, перекрестное связывание является важнейшим механизмом, замедляющим распад дермальных филлеров, содержащих ГК. В дермальных филлерах на основе ГК, представленных на рынке США, в качестве молекул-сшивок используются 2 вещества: 1,4-бутандиол-диглицидиловый эфир (BDDE) и дивинилсульфон (DVS). Оба вещества реагируют с гидроксильными группами цепей ГК и одинаково эффективно замедляют ферментную и свободнорадикальную деградацию дермальных филлеров после их введения в кожу. На рисунке 5 продемонстрировано, как молекула-сшивка BDDE связывает 2 полимерные цепи ГК.
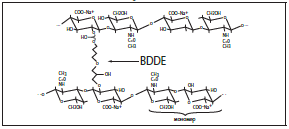
Рисунок 5. Молекула-сшивка BDDE (1,4-бутандиолдиглицидиловый эфир), используемая для того, чтобы связать полимерные цепи ГК между собой и превратить жидкий раствор ГК в гель. Прореагировать c BDDE способны как первичная гидроксильная группа (-CH2OH), так и вторичная гидроксильная группа (-CHOH) каждого мономера ГК.
После перекрестного связывания цепей ГК в конечном продукте может содержаться некоторое остаточное количество непрореагировавших молекул кросслинкера. Остаточные молекулы вещества-сшивки представляют собой артефакты процесса производства и в высоких концентрациях могут быть токсичными. Их присутствие крайне нежелательно, и производители дермальных филлеров предпринимают особые меры для того, чтобы устранить как можно большее количество непрореагировавших молекул-сшивок из конечного продукта.
Для того чтобы гарантировать безопасность дермальных филлеров, производимых в США, Управление по контролю за продуктами и лекарствами считает, что концентрация остаточного вещества-сшивки в дермальных филлерах должна быть на несколько порядков ниже уровня, который может вызывать беспокойство за здоровье человека.
Степень перекрестного связывания
Сравнивая дермальные филлеры на основе ГК, важно хорошо представлять себе значение понятия «степень перекрестного связывания». Степень перекрестного связывания указывает, какая доля мономерных дисахаридных остатков в цепи ГК связана с молекулами-сшивками. Так, говоря о том, что степень перекрестного связывания в дермальном филлере составляет 4%, подразумевают, что на каждые 100 дисахаридных остатков в полимерной цепи ГК приходится в среднем 4 молекулы-сшивки (рисунок 6).
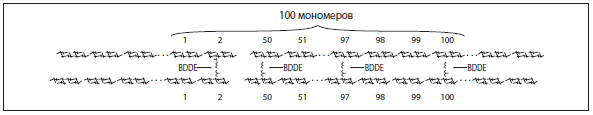
Рисунок 6. Степень перекрестного связывания. Если на каждые 100 дисахаридных мономеров приходится 4 связи с BDDE, степень перекрестного связывания составляет 4%. Точная локализация мономеров, прореагирующих с BDDE, определяется статистически в процессе реакции. На рисунке представлен один возможный вариант из множества.
При неизменности других параметров справедливо правило, что чем больше степень перекрестного связывания, тем тверже гель. Важность твердости (или мягкости) геля будет обсуждаться в дальнейших разделах статьи.
Говоря о степени перекрестного связывания, необходимо понимать, что многие дермальные филлеры на основе ГК состоят как из перекрестно-связанных, так и перекрестно не связанных фаз (далее в статье под перекрестно не связанной ГК понимают ту порцию продукта, которая содержит как перекрестно не связанные цепи, так и незначительно перекрестно связанные цепи и фрагменты, которые будут уменьшать силу выдавливания и облегчать распределение препарата; эти незначительно перекрестно связанные цепи и фрагменты в организме будут вести себя так же, как и перекрестно не связанная ГК – то есть, облегчая выдавливание и распределение препарата, внесут лишь ограниченный вклад в коррекцию морщин, либо не обеспечат ее вообще). По определению степень перекрестного связывания характеризует только ту долю ГК, которая действительно вступила в реакцию. Именно перекрестно связанная ГК обеспечивает волюмизирующий эффект дермального филлера в коже, в то время как перекрестно не связанная ГК выводится из организма за несколько дней.
При прочих равных факторах для дермальных филлеров на основе ГК справедливо правило, что большая степень перекрестного связывания клинически проявляется более длительным сохранением филлера в коже. В то же время, существует пока еще точно не определенное пороговое значение степени перекрестного связывания, при превышении которого степень гидрофильности (сродства к воде) полимерных цепей ГК, а следовательно и лифтинговый потенциал геля, могут снизиться (см. раздел «Концентрация и степень гидратации»). Кроме того, превышение этого порогового значения может изменить биосовместимость продукта и вызвать иммунную реакцию на введенный гель ГК: вместо того, чтобы постепенно расщеплять его, организм может начать отторжение геля, что вызовет нежелательные реакции, например инкапсуляцию и формирование гранулемы или стерильного абсцесса.
Принимая во внимание вышеперечисленное, производители дермальных филлеров стараются не приближаться к этому пороговому значению и добиваются баланса между той степенью перекрестного связывания полимерных цепей ГК, которая позволила бы добиться длительного сохранения эффекта, в тоже время гарантируя отсутствие каких-либо нежелательных явлений, в частности реакции отторжения.
Твердость геля
Твердость геля характеризует прочность препарата ГК, а точнее его устойчивость к деформации. Специалисты в области химии полимеров используют для количественной оценки твердости геля величину G` – модуль упругости [7]. В твердость геля, измеряемую в G`, в конечном итоге вносят вклад и концентрация ГК, и степень перекрестного связывания, и количество перекрестно не связанной ГК, и процесс производства.
Твердость геля можно проиллюстрировать на следующем примере: если гель ГК поместить между двумя плоскостями, а затем верхнюю плоскость быстро сдвинуть в горизонтальном направлении на небольшое расстояние, сохраняя нижнюю неподвижной, потребуется сила, чтобы удержать возникшую деформацию сдвига на месте. G` определяют как отношение напряжения сдвига (силы на единицу действия площади поверхности) к произведенной деформации сдвига (отношения горизонтального смещения к вертикальному расстоянию между плоскостями). В геле с низкой степенью перекрестного связывания, где полимерные цепи ГК связаны между собой непрочно, сила, которую необходимо приложить для смещения, невелика, поэтому твердость геля или G` мала. При увеличении степени перекрестного связывания и той же средней концентрации ГК, сеть, состоящая из полимеров ГК, становится более прочной, и для смещения геля требуется приложить большую силу, поэтому твердость геля или G` возрастает (рисунок 7).
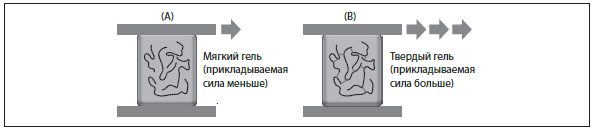
Рисунок 7. Твердость геля (модуль упругости G`). Значение G` определяют, помещая гель между двумя плоскостями и смещая верхнюю плоскость в горизонтальном направлении относительно нижней. Для 2 продуктов с одинаковой концентрацией ГК справедливо правило, что чем меньше степень перекрестного связывания, тем мягче гель и тем меньше значение G`.
(A) Мягкий гель (прикладываемая сила меньше) (B) Твердый гель (прикладываемая сила больше)
Такое определение твердости геля справедливо в отношении монолитной гелевой массы, которую получают после завершения реакции перекрестного связывания в растворе полимера ГК. Далее будет подробно обсуждаться, что один из этапов процесса производства дермальных филлеров на основе ГК заключается в дроблении гелевой массы на мелкие частицы для того, чтобы препарат можно было ввести в кожу с помощью иглы. Препараты на основе ГК, содержащие частицы с большими значениями G` сложны для введения, даже если гелевые частицы в конечном продукте очень малы по размеру. Для того чтобы преодолеть это затруднение, некоторые производители дермальных филлеров добавляют препарат перекрестно не связанную ГК в качестве своего рода «любриканта», снижающей G` во время введения препарата и, таким образом, уменьшающей силу, которую необходимо приложить для проведения инъекции. Однако хотя перекрестно не связанная ГК и позволяет сделать инъекции дермального филлера более легкими, она сохраняется в организме лишь в течение непродолжительного времени и, таким образом, не вносит вклад в длительный эстетический эффект.
Консистенция геля гиалуроновой кислоты
Важной характеристикой, оказывающей влияние на клинические свойства дермального филлера, является размер частиц геля в конечном продукте. Как уже обсуждалось выше, процесс создания дермальных филлеров на основе ГК напоминает приготовление желе – смешивание желатинового порошка с горячей водой и охлаждение раствора, после чего он превращается в однородную гелевую массу. Эту гелевую массу затем необходимо «измельчить», чтобы конечный продукт можно быть ввести в кожу. Измельчение достигается путем просеивания гелевой массы через несколько решетчатых фильтров или сит. Дермальные филлеры на основе ГК, которые производят подобным методом, содержат гелевые частицы четко определенного среднего размера. Величина гелевых частиц в различных продуктах неодинакова и определяется тем, какой метод просеивания использовался в процессе производства. Существует максимальный размер частиц дермального филлера, при превышении которого возникает вероятность, что филлер будет выдавливаться из шприца с затруднением, а игла во время инъекции будет забиваться.
Кроме того, существует связь между размерами частиц и скоростью их расщепления в организме. Крупные частицы ГК обладают меньшей суммарной площадью поверхности (площадь на объем геля), с которой способны взаимодействовать расщепляющие их ферменты, имеющие сравнительно большие размеры и трудно проникающие в «сеть» полимерных молекул, из которой состоят гелевые частицы. Частицы ГК меньших размеров характеризуются большей суммарной площадью поверхности, с которой способны взаимодействовать ферменты, и процесс расщепления протекает быстрее. В противоположность этому, скорость расщепления гелевых частиц под действием свободных радикалов, повидимому, в меньшей степени зависит от их размеров, поскольку многие свободные радикалы малы и легко проникают внутрь геля. Тем не менее, при прочих равных, в том числе и при равном объеме геля, скорость расщепления продукта в организме и его исчезновения будет выше у того филлера, где средняя величина частиц меньше (рисунок 8).
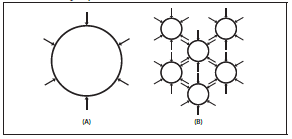
Рисунок 8. Размер частиц и скоростью расщепления.
Теоретически, чем больше размер частиц геля (А), тем меньше суммарная площадь поверхности, с которой способны взаимодействовать ферменты организма, расщепляющие ГК. Чем меньше размер частиц (В), тем больше суммарная площадь поверхности, доступная для контакта. При прочих равных, если частицу большого размера (А) раздробить на несколько более мелких частиц (В) так, что суммарный объем останется неизменным, теоретически большая суммарная площадь поверхности совокупности мелких гелевых частиц будет более активно атаковаться ферментами и поэтому филлер будет быстрее расщепляться в коже. Однако в связи с пористостью частиц геля ГК, влияние их размера на клинические свойства препарата очень невелико, поскольку ферменты способны проникать в гель и разрушать его не только снаружи, но и изнутри.
Однако, принимая во внимание достаточно малые различия размеров гелевых частиц в препаратах, одобренных для применения в США, отличия скорости расщепления могут быть не столь велики, чтобы как-либо проявиться с клинических позиций.
Альтернативным методом измельчения гелевой массы является гомогенизация, в результате которой конечный продукт приобретает однородную консистенцию и по внешним характеристикам напоминает густой яичный белок, в отличие от более зернистой консистенции обсуждавшихся выше препаратов, содержащих частицы геля. Возможно, однородная консистенция является следствием гораздо большего разброса размеров гелевых частиц, по сравнению с получаемым после просеивания. Продукты, которые производятся с помощью этой технологии, представляют собой более мягкие гели с меньшими значениями G`, легко распределяющиеся под кожей, что позволяет отказаться от использования фильтров, которые в процессе производства искусственно устраняют из препарата частицы, размер которых превосходит максимально допустимый. Эти препараты получили одобрение Управления по контролю за продуктами и лекарствами США недавно и сочетают в себе продолжительность эффекта и простоту введения.
Вязкость, эластичность и сила выдавливания
Мы обсудили понятие твердости геля G`, характеризующее силу, которую необходимо приложить, чтобы произвести его небольшую и резкую деформацию. Таким образом, величина G` предоставляет информацию о линейных упругих свойствах геля. Однако с клинических позиций более важен показатель силы выдавливания, которую врач должен приложить, чтобы ввести филлер, содержащий ГК, в мягкие ткани через иглу. Схематичное изображение кривой силы выдавливания представлено на рисунке 9, где F (сила, которую необходимо приложить к поршню шприца, чтобы ввести дермальный филлер) представляет собой функцию от D (расстояние, на которое смещается поршень шприца).
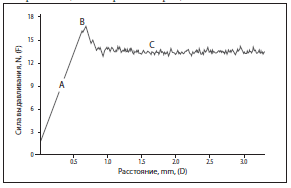
Рисунок 9. Сила F, которую необходимо прикладывать, чтобы смещать поршень шприца, заполненного дермальным филлером на основе ГК на расстояние D с постоянной скоростью. Участок (А) соответствует эластическому режиму, и угол наклона кривой пропорционален твердости геля G`; точка (B) – предел текучести, при которой гель начинает поступать из шприца, а участок (С) соответствует вязкому режиму, при котором F по мере увеличения D практически не изменяется и зависит от вязкости филлера.
График построен исходя из условия, что давление на поршень осуществляется непрерывно, что соответствует плавному постоянному введению препарата. Первоначально сила возрастает в линейной зависимости от смещения D, и этот режим носит название линейно-упругого. Фактически, угол наклона линии при таком режиме пропорционален твердости геля G`. В том случае, если гель твердый, по мере смещения поршня требуемая сила выдавливания будет увеличиваться резко, а врач почувствует, что ему трудно заставить поршень продвигаться.
По мере того, как смещение продолжает увеличиваться, кривая F-D утрачивает линейный вид, и гель становится текучим и подвергается пластической деформации. После максимальной точки на кривой F-D, которая носит название предела текучести, гель начинает поступать в точку инъекции и сила выдавливания постепенно уменьшается. Наконец, дальнейшее смещение поршня приводит к переходу в режим вязкости, при котором по мере увеличения D значение F практически не изменяется, и филлер с постоянной скоростью поступает в ткани. При этом режиме постоянная сила, которую необходимо прикладывать для введения препарата, определяется вторым физическим параметром – вязкостью (η). Необходимо отметить, что если в любой момент процедуры врач прекратит вводить препарат, ему или ей при возобновлении инъекции придется вновь повторить всю кривую зависимости F от D. Таким образом, вводя содержимое шприца в несколько приемов, требуется прикладывать больше усилий, чем при одной непрерывной инъекции.
Вязкость дермального филлера и сила, которую необходимо приложить, чтобы выдавить продукт из шприца через иглу, зависит от степени перекрестного связывания, количества перекрестно связанных и не связанных цепей ГК в конечном продукте, метода измельчения, средней величины гелевых частиц и разброса их размеров, а также от процесса производства как такового. При неизменности прочих факторов, увеличение степени перекрестного связывания делает гель более твердым, а также повышает его вязкость и силу выдавливания. Подобно этому, при неизменности иных факторов, продукты, произведенные с использованием решетчатых фильтров для создания гелевых частиц с точно заданными размерами, также обладают большей вязкостью и силой выдавливания, чем продукты однородной консистенции с широким разбросом величин гелевых частиц.
Крайне важную роль в текучести дермальных филлеров и их инъекционных характеристиках играет перекрестно не связанная ГК. Линейные или перекрестно не связанные молекулы ГК обладают хорошей смазывающей способностью. Именно эта характеристика и позволяет перекрестно не связанной ГК облегчать введение геля в кожу через тонкую иглу. Продукты с небольшим разбросом размеров гелевых частиц – например, производимые с помощью метода просеивания – плохо выдавливаются из шприца (вследствие значительной силы выдавливания и высокой вязкости) до тех пор, пока в состав конечного продукта не будет введено значительное количество перекрестно не связанной ГК. Однако, как уже обсуждалось выше, единственным свойством перекрестно не связанной ГК является облегчение введения продукта. Перекрестно не связанная ГК быстро метаболизируется в коже и, таким образом, не вносит вклад в конечный сохраняющийся в течение более длительного времени эстетический результат. Новые филлеры на основе ГК, при производстве которых используются современные методы измельчения, позволяющие добиться большого разброса размеров частиц и однородной консистенции филлера, обладают преимуществом вследствие того, что для проведения инъекции и более равномерного распределения препарата требуется включение в его состав меньшего количества перекрестно не связанной ГК. Таким образом, эти продукты содержат большую долю перекрестно связанной ГК, которая сохраняется в коже, что может повысить стойкость эффекта и улучшить клинические исходы.
Концентрация и степень гидратации
Одним из наиболее важных свойств ГК, которое делает возможным ее использование в качестве дермального филлера, является способность увеличиваться в объеме, притягивая большое количество воды, благодаря полианионной и водород-связывающей природе молекулы. 1 грамм геля, состоящего из цепей слабо перекрестно связанной ГК, способен связать до 3 литров воды, что сопоставимо со свойствами гелей полиакриламидной кислоты, которые используются в качестве сверхактивных адсорбентов в современных подгузниках.
Равновесие гидратации геля ГК достигается, когда осмотические силы, связанные с его гидрофильной природой, уравновешивают эластические силы набухшей сети молекул ГК. Продукты, характеризующиеся традиционными степенями перекрестного связывания и концентрацией ГК приблизительно 5,5 мг/мл воды, близки к состоянию равновесия гидратации. При введении этих продуктов в кожу они не будут дополнительно набухать, поскольку уже насыщены водой. В то же время, продукты, содержащие более высокие концентрации ГК (от 20 до 24 мг/мл) не находятся в состоянии равновесия гидратации. Эти препараты будут немного увеличиваться в объеме после введения в кожу, притягивая воду из окружающих тканей. Слегка не достигать равновесия гидратации – благоприятная характеристика для дермального филлера, поскольку она будет обеспечивать желаемый волюмизирующий эффект. Однако для того, чтобы это свойство правильно реализовывало все свои преимущества в клинической практике, врач, осуществляющий инъекции, должен быть хорошо знаком с характеристиками каждого конкретного продукта для того, чтобы конечный эстетический результат был адекватным.
Резюме
Существуют несколько химических и физических характеристик, которые влияют на конечные свойства готового дермального филера на основе ГК (таблица 1).

Выводы
Современные дермальные филеры на основе ГК эффективно восстанавливают утраченный объем, благодаря своей гидрофильности. Хотя длительное сохранение эффекта от действия препарата и представляется важной характеристикой, главными свойствами, по которым оценивают продукт, являются чистота, безопасность, простота введения и комфорт для пациента. Подбирая дермальный филлер, крайне важно представлять себе с научных позиций связь его химических и физических характеристик с вышеперечисленными свойствами [8]. С точки зрения влияния на пациента при использовании большинства дермальных филлеров наиболее важна безопасность каждого конкретного препарата, однако впечатление, которое останется у пациента в целом, будет зависеть от того, как пройдет лечение от начала до конца: от момента консультации и дачи информированного согласия до завершения периода восстановления и оценки полученного результата. Необходимо ознакомить пациентов с особенностями проведения эстетической коррекции на различных участках, требуемым объемом препарата (и его стоимостью), чтобы их ожидания были реалистичными, и они покидали бы клинику с чувством удовлетворенности [9].
Представленные сегодня на рынке дермальные филлеры на основе ГК хотя и приближаются по своим характеристикам к «идеальному» филлеру для эстетического омоложения, все еще характеризуются ограничениями, cвязанными с простотой введения препарата и длительностью его сохранения в организме. Необходим тщательный мониторинг нежелательных явлений, возникающих на фоне применения новых препаратов, появляющихся на рынке, хотя большинство из этих явлений и являются местными, слабо выраженными и преходящими. Особого опыта и внимания врача требуют два направления: удовлетворение ожиданий пациентов и их поддержка после процедуры введения препарата – и при правильном подходе к этим вопросам исходы лечения становятся превосходными [4].
Новые дермальные филлеры на основе ГК, недавно одобренные Управлением по контролю за продуктами и лекарствами для применения в США, с уникальными химическими и физическим свойствам по заявлениям производителей должны на шаг приблизить нас к идеальному филлеру. В свете появления на рынке этих новых препаратов и расширения возможностей выбора как для начинающих, так и для опытных специалистов становится все более важным хорошо разбираться в тех основных свойствах дермального филлера на основе ГК, которые играют роль в его клинических характеристиках, особенно в простоте использования, эффективности в достижении оптимального результата и длительности действия, а также в вопросах безопасности с точки зрения снижения частоты таких нежелательных явлений, как появление гематом, отеков и боли.
Наконец, нельзя не упомянуть, что ничто не способно заменить тех бесценных знаний, которые можно получить, наблюдая за опытным специалистом или посещая мастер-классы [8]. Для того чтобы гарантировать достижение тех результатов, которыми будут довольны пациенты, понимание химических и физических свойств дермальных филлеров на основе ГК должно сочетаться с правильной техникой и необходимым опытом.
Литература:
1. American Society of Plastic Surgeons. Injectable fillers: Improving skin texture. Arlington Heightsm IL: American Society of Plastic Surgeons4 2006. Accessed: June 22, 2006. URL: http://www.plasticsurgery.org/pulic_education/prodecures/ InjectabeFillers.cfm.
2. Dover JS. The filler revolution has just begum. Plast Reconst Surg. 2006;117(3 suppl):38S.
3. Niamtu J. III. The use of restylane in cosmetic facial surgery. J Oral Maxillofac Surg. 2006 Feb;64(2):317-25.
4. Matarasso SL, Carruthers JD, Jewell ML; Restylane Consensus Group. Consensus recommendations for soft-tissue augmentation with nonanimal stabilized hyaluronic acid (Restylane). Plast Reconstr Surg. 2006 Mar;117(3 Suppl):3S-34S.
5. Monheit GD, Coleman KM Hyaluronic acid fillers. Dermatol Ther. 2006 May-Jun;19(3):141-50.
6. Matarasso SL. Practice forum: Understanding and using hyaluronic acid. Aesthetic Surg J. 2004;24:361-4.
7. Ferry JD. Viscoelastic properties of polymers. 3rd ed. New York: John Wiley & Sons, Inc; 1980.
8. Klein AW. The art and science og injectable hyaluronic acids. Plast Reconstr Surg. 2006 117(3 Suppl):35S.
9. Fagien S. The Restylane consensus statement. Plast Reconstr Surg. 2006 117(3 Suppl):41S.
