Че-Ён Пак, MD* Ниамх Кордафф, MBBS† Юрген Фреверт, PhD
Рунгсима Ванитпхакдидеча,MD, MA, MSc
Йейтс И. И. Чао, MD
Актуальность. В составе большинства препаратов ботулинического токсина типа A (БТА) присутствуют необязательные бактериальные компоненты, которые повышают риск выработки нейтрализующих антител (НАТ). С выходом на рынок новых препаратов БТА стали появляться сообщения о случаях вторичной неэффективности лечения (ВНЛ) вследствие образования НАТ.
Методы. Чтобы сформулировать рекомендации по ведению пациентов в случае развития устойчивости к токсину, был проведен опрос среди 128 экспертов Азиатского региона, регулярно выполняющих инъекции ботулотоксина. По результатам опроса были рассмотрены данные по иммуногенности БТА, проведена оценка текущей клинической практики азиатских врачей, а также рассмотрены современные научные знания и данные реального клинического опыта применения БТА.
Результаты. Большинство врачей считают, что случаи ВНЛ возможны, при этом у некоторых пациентов отмечается неполная эффективность, а примеси (например, комплексообразующие белки) в препаратах БТА повышают риск развития ВНЛ. Биологические методы анализа, позволяющие отличить АТ, не обладающие нейтрализующей активностью, от НАТ, препятствующих действию токсина, остаются недоступны для многих врачей, хотя большинство специалистов готовы использовать их на практике при наличии такой возможности. Врачи в Азиатско-Тихоокеанском регионе используют различные стратегии ведения пациентов с ВНЛ в зависимости от наличия альтернативных методов лечения или доступности анализов. Они рекомендуют перейти на высокоочищенный препарат, не содержащий комплексообразующих белков и других примесей, чтобы снизить иммуногенность, или предлагают пациенту перерыв в лечении длительностью 2–2,5 года. Кроме того, при возобновлении терапии также предлагается применять высокоочищенный препарат. Это особенно важно при проведении повторных курсов, при введении высоких доз, а также у более молодых пациентов, которые в течение жизни вероятно получат высокую кумулятивную дозу БТА. Подобная стратегия позволяет минимизировать иммуногенность и сохранить долгосрочные результаты лечения. Важно отметить, что с самого начала терапии всегда следует отдавать предпочтение именно высокоочищенным препаратам, не дожидаясь развития резистентности.
Заключение. Выбор в пользу высокоочищенных препаратов БТА в начале лечения повышает долгосрочную эффективность терапии и удовлетворенность пациентов, сводя к минимуму риск активации иммунной системы и образования НАТ. (Plast Reconstr Surg Glob Open 2022;10:e4217; doi: 10.1097/GOX.0000000000004217; Published online 18 April 2022.)
ВВЕДЕНИЕ
За последний год1–3 рост количества новых препаратов ботулинического токсина типа A (БТА), применяемых по эстетическим показаниям, сопровождается появлением отдельных сообщений о побочных эффектах, связанных с БТА, и неблагоприятных результатах лечения. К хорошо изученным препаратам БТА относятся онаботулотоксин A (онаА; Ботокс, «Аллерган Инк.», Ирвин, Калифорния), абоботулотоксин A (абоА; Диспорт, «Ипсен Лтд.», Слау, Беркшир, Великобритания) и инкоботулотоксин A (инкоА; Ксеомин, «Мерц Фармасьютикалс ГмбХ», Франкфурт-на-Майне, Гессен, Германия). К новым препаратам, используемым в Азиатско-Тихоокеанском регионе (АТОР), относятся летиботулотоксин A (Ботулакс, «Хюгель Фарма», Сеул, Корея), пработулотоксин A (Набота, «Дэвунг Фармасьютикалз», Сеул, Корея), Иннотокс и Медитоксин («МедиТокс Инк.», Сеул, Корея), Гутокс («Хуонс Ко. Лтд.», Кёнгидо, Корея), Релатокс («Микроген», Россия) и Лантокс (Институт биологических препаратов Ланьчжоу, Китай)4. Ожидается регистрация и выход на рынок Кореи препаратов Протокс («ПРОТОКС Инк.», Сеул, Корея) и ЗэТоксин («Джетема Инк.», Сеул, Корея).
Все чаще врачи сталкиваются с вторичным отсутствием ответа или так называемой «резистентностью к токсину» из-за образования нейтрализующих антител (НАТ) к БТА после применения препарата по эстетическим показаниям5–12. Вторичная неэффективность лечения (ВНЛ) определяется как потеря или снижение клинической эффективности после первоначального ответа на БТА13, развивающаяся со временем на фоне повторных инъекций14. Подозрение на частичную ВНЛ (ЧВНЛ) может возникнуть при необходимости введения более высоких доз БТА для достижения того же клинического эффекта («дрейф» дозы) или при сокращении продолжительности эффекта на фоне неизменной дозы («дрейф» интервала). Полное отсутствие клинического ответа на любое количество введенного БТА считается полной ВНЛ (ПВНЛ).
Тест защиты мышей* и мышиный гемедиафрагмальный тест† являются современным стандартом оценки уровня НАТ к БТА14. Хотя стандартные структурные иммунологические анализы связывания, такие как твердофазный иммуноферментный анализ и анализ иммунопреципитации, обладают необходимой чувствительностью для обнаружения антител к БТА, они не позволяют отличить антитела, не обладающие нейтрализующей активностью, от НАТ, препятствующих эффективному действию препарата. В рамках данной работы была оценена ситуация в АТОР с учетом опубликованных данных по иммуногенности БТА и современных принципов применения БТА, которыми врачи в АТОР руководствуются в своей практике. Затем 24 июля 2020 года была проведена виртуальная конференция АТОР, чтобы выявить пробелы в знаниях, обменяться реальным клиническим опытом и взглядами, а также сформулировать рекомендации по ведению пациентов с устойчивостью к токсину.
МЕТОДЫ
Опрос проводили среди специалистов АТОР, регулярно выполняющих инъекции ботулинического токсина (n = 128; группа «экспертов»). Среди участников опроса были дерматологи, пластические хирурги и врачи-косметологи с широким опытом применения БТА, которые регулярно использовали два или более препарата БТА. Эти специалисты получили по электронной почте анкету (услуга компании «СёвиМанки Инк.»; www.surveymonkey.com) с вопросами о текущей клинической практике, опыте применения БТА и видении проблемы неэффективности лечения на фоне образования НАТ, о применении БТА по другим медицинским показаниям в зонах помимо лица, а также с целью улучшения качества кожи (внутрикожно — мезотоксин). Кроме того, специалистов спросили об их опыте работы с препаратами нейротоксина, произведенными в Азии. После этого 38 экспертов, пожелавших поделиться своим мнением, были приглашены на виртуальную конференцию, чтобы обсудить ответы.
РЕЗУЛЬТАТЫ
Важно отметить, что формирование консенсуса для конкретных стран АТОР, регионов, клинической практики или предпочтений не являлось целью данного исследования, и оно не обладает соответствующей статистической мощностью. Представленные здесь ответы скорее отражают общие взгляды врачей, клинические аспекты и применяемые на практике методы решения проблемы иммуногенности. Из 128 опрошенных экспертов 38 приняли участие в виртуальной конференции для обсуждения ответов.
Основные положения
Вопрос. Сообщения о случаях вторичной неэффективности лечения (ВНЛ) вследствие образования нейтрализующих антител (НАТ) послужили поводом для анализа данных по иммуногенности ботулотоксина типа A (БТА), изучения клинической практики, научных знаний и реального опыта азиатских врачей, а также для разработки рекомендации по ведению пациентов при развитии устойчивости к ботулиническому токсину.
Результаты. Большинство врачей считают, что случаи ВНЛ возможны, при этом у некоторых пациентов отмечается неполная эффективность, а примеси (например, комплексообразующие белки) в препаратах БТА повышают риск развития ВНЛ. Врачи Азиатско-Тихоокеанского региона дали рекомендации по решению этой проблемы, и в том числе отметили, что с самого начала терапии всегда следует отдавать предпочтение именно высокоочищенным препаратам, не дожидаясь развития резистентности.
Значение. Выбор в пользу высокоочищенных препаратов БТА в начале лечения повышает долгосрочную эффективность лечения и удовлетворенность пациентов, сводя к минимуму риск активации иммунной системы и образования НАТ.
Вторичная неэффективность лечения и нейтрализующие антитела
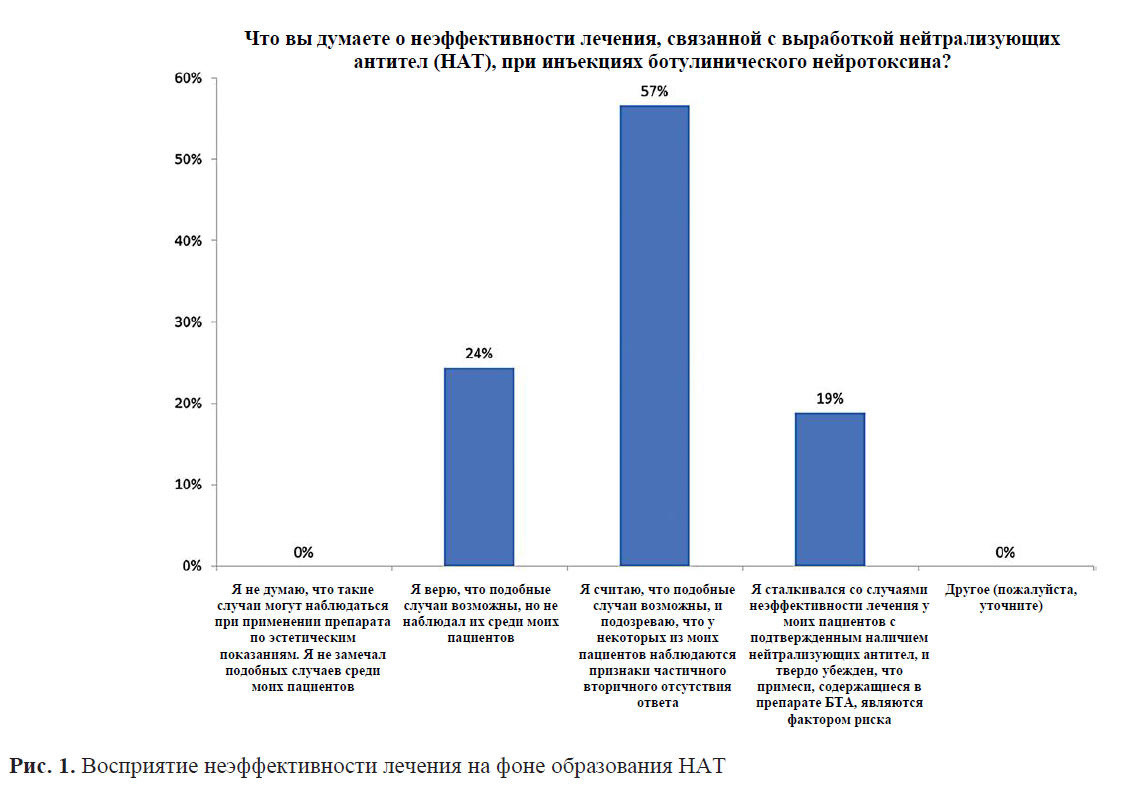
Более половины (57 %) экспертов считают, что у пациентов может развиться ПВНЛ или ЧВНЛ, и полагают, что на данный момент симптомы ЧВНЛ отмечаются у некоторых из их пациентов (рис. 1). Важно отметить, что 19 % экспертов, столкнувшихся с ВНЛ на практике, твердо убеждены, что значимым фактором ее развития являются примеси (в частности, комплексообразующие белки, инактивированные нейротоксины, флагеллины и бактериальная ДНК)15, содержащиеся в препаратах БТА. Четверть экспертов не сталкивались с ВНЛ. Для понимания влияния определенных методик или самих препаратов БТА на результат необходимы дальнейшие исследования.
Анализ для выявления НАТ
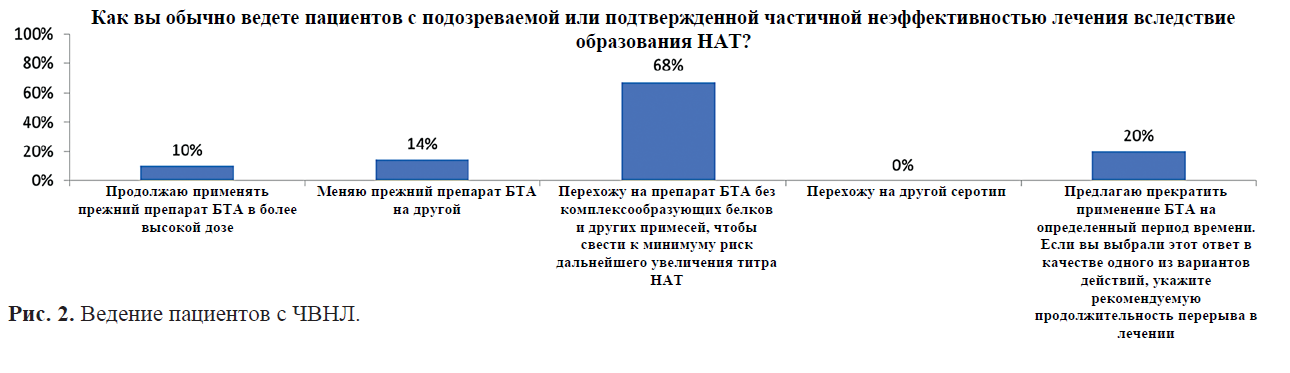
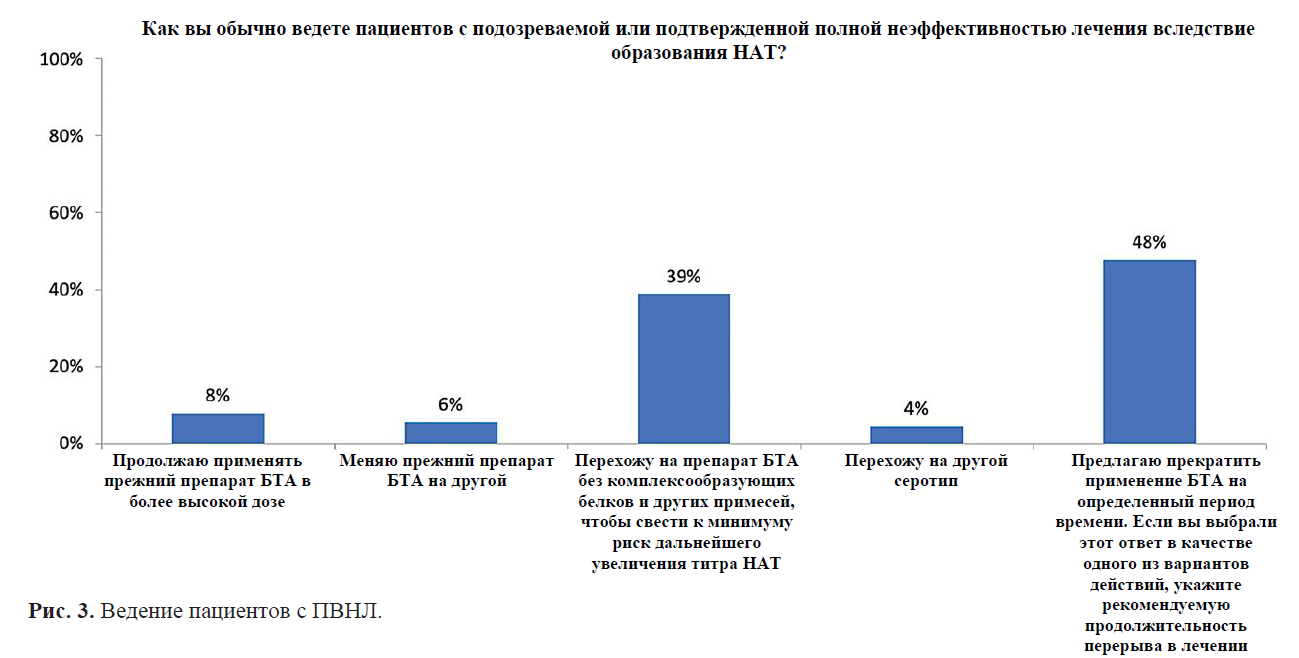
Анализ для выявления НАТ не имели возможности выполнить 68 % экспертов (эти данные не представлены графически), при этом большинство экспертов (83,3 %) провели бы такое обследование при подозрении на ЧВНЛ или ПВНЛ (если бы это было технически возможно в их стране). Остальные 16,7 % не сочли нужным проводить анализ на НАТ и отметили, что не стали бы менять план лечения независимо от результатов обследования. Чтобы скорректировать ЧВНЛ или ПВНЛ, эксперты готовы перейти на препарат, не содержащий комплексообразующих белков и других примесей, что снижает риск дополнительной иммуногенности (68 % в случае ЧВНЛ, рис. 2; 39 % в случае ПВНЛ, рис. 3), или предложить пациенту на время прервать лечение (20 % в случае ЧВНЛ, рис. 2; 48 % в случае ПВНЛ, рис. 3). Некоторые из экспертов готовы перейти на препараты, отличные от инкоА (14 % в случае ЧВНЛ, рис. 2; 6 % в случае ПВНЛ, рис. 3), или увеличить дозу уже применяемого препарата (10 % в случае ЧВНЛ, рис. 2, 8 % в случае ПВНЛ, рис. 3). Такие ответы могут отражать упорное желание некоторых пациентов продолжать терапию.
Мезотоксин для коррекции мимических морщин
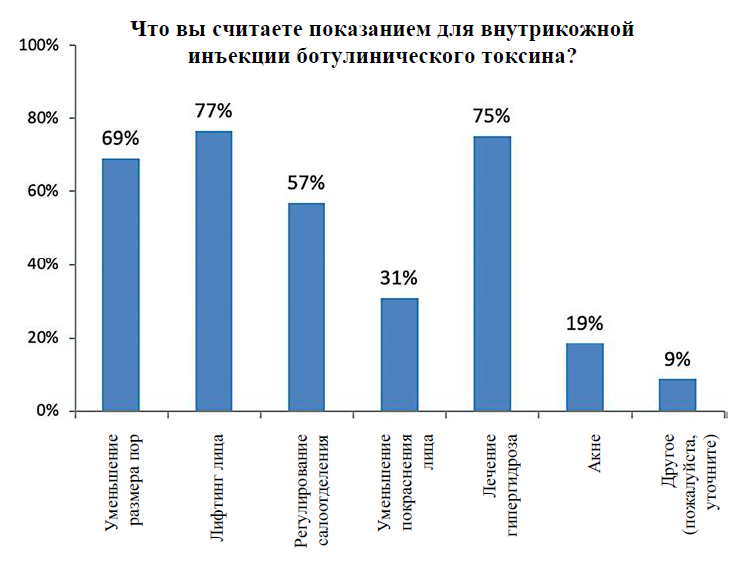
Внутрикожные инъекции ботулинического токсина применяются для лифтинга тканей лица, коррекции гипергидроза, уменьшения размера пор, регулирования салоотделения, уменьшения покраснения лица, лечения акне и по другим показаниям (перечислены в порядке уменьшения частоты использования) (рис. 4). Примечательно, что 54 % экспертов считают внутрикожные инъекции более иммуногенными, чем внутримышечные (данные не представлены графически). Это может быть связано с известным фактом, что дендритные клетки, осуществляющие захват антигена, расположены преимущественно в дерме16. Кроме того, 94 % экспертов считают важным применять для внутрикожных инъекций высокоочищенные, не содержащие комплексообразующих белков препараты БТА с наименьшей иммуногенностью.
Показания для применения в других зонах тела, помимо лица
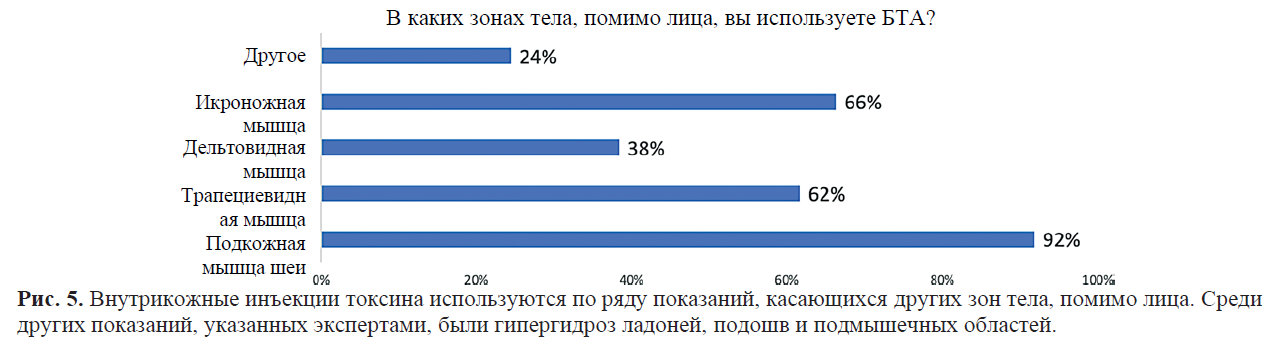
Почти все эксперты (96 %, данные не представлены графически) используют БТА для введения в мышцы тела, помимо лица, включая трапециевидную и икроножную мышцы (рис. 5). Считается, что при введении в другие зоны тела БТА оказывает более выраженное иммуногенное действие (65 %), в основном ввиду более высоких доз (например, > 100 ед.). По этой причине 97,1 % экспертов считают важным использовать для введения в мышцы тела, помимо лица, высокоочищенные препараты с наименьшей иммуногенностью.
Опыт применения препаратов БТА, производимых в Азии, врачами АТОР
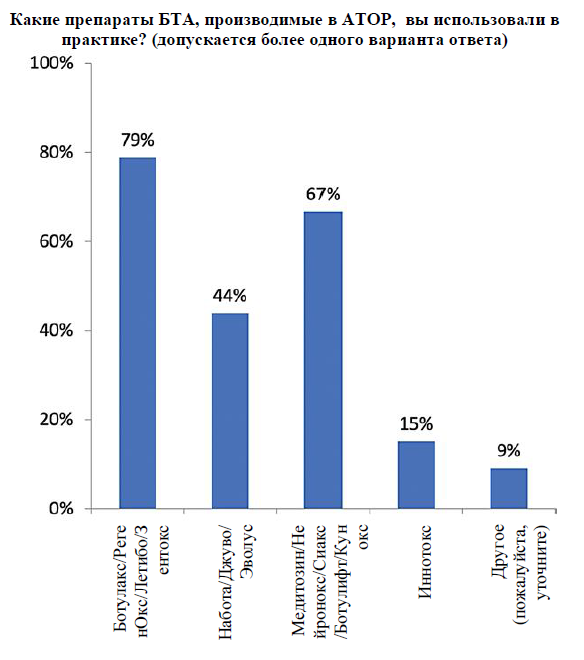
В целом, 73 % экспертов используют в своей практике азиатские бренды БТА, включая Ботулакс (также известный как РегенОкс, Летибо или Зентокс, 79 %; рис. 6), Медитоксин (также известный как Нейронокс, Ботулифт, Кунокс или Сиакс, 67 %) и Набота (также известный как Джуво или Нусива, 44 %). Менее 20 % применяют Иннотокс. Важно отметить, что 88 % экспертов считают высокое содержание примесей в препаратах БТА азиатского производства фактором, повышающим риск развития ВНЛ вследствие образования НАТ (данные не представлены графически).
ОБСУЖДЕНИЕ
После опроса эксперты из АТОР обсудили аспекты терапевтической практики и перспективы в отношении проведения анализов на антитела, целесообразности перерывов в лечении и замены препаратов, внутрикожного и внутримышечного введения, а также обменялись опытом использования новых препаратов БТА азиатского производства. Необходимо подчеркнуть, что из-за различий между странами полученные в опросе ответы не могут рассматриваться как консенсус. Во избежание искажения полученных данных эта статья не содержит выводы о лечебной практике, применяемой в отдельных странах. Цель данной работы — обзор проблемы иммуногенности, связанной с БТА, и реального опыта сообщества специалистов эстетической медицины в АТОР.
Поскольку последствия иммуногенности БТА были сходными во всем АТОР, полученные нами результаты имеют определенную значимость и подчеркивают необходимость тщательного выбора препарата ботулинического токсина, потребность в разработке регламентированных стратегий контроля ВНЛ и/или тактик ведения пациентов, настаивающих на длительном лечении. Дополнительные исследования иммуногенности токсина могли бы выявить связь с различными терапевтическими подходами, предпочтениями и особенностями, характерными для различных регионов (например, в Восточной Азии и Юго-Восточной Азии) или стран (например, в Корее и Тайване). Более структурированное консенсусное мнение (например, с использованием дельфийского метода) облегчило бы врачам, ведущим клиническую практику, понимание результатов данного исследования и могло бы служить в качестве практических рекомендаций. Будущие исследования, в частности продольные исследования в условиях реальной клинической практики и клинические регистры, дополнят полученные данные и позволят лучше понять сложную, динамически развивающуюся и малоизученную проблему иммуногенности БТА в эстетической медицине.
Ниже в обобщенном виде представлен наш клинический опыт, связанный с иммуногенностью ботулинических токсинов. Эти сведения могут не иметь прямого отношения к опросу экспертов в связи с неформальным характером виртуальной конференции.
ПРИМЕНЕНИЕ ИНКОБОТУЛОТОКСИНА А В КЛИНИЧЕСКОЙ ПРАКТИКЕ
Хотя опыт, полученный экспертами из АТОР, в целом сходен, применяемые ими стратегии лечения различаются в зависимости от наличия альтернативных методов терапии или оборудования для анализа на наличие антител.
1. Так, в Корее анализ на антитела обычно не проводится; вместо этого случаи с подозрением на ВНЛ подтверждают с помощью теста на сократимость лобной мышцы. Поскольку непрерывная терапия на фоне полного отсутствия ответа неэффективна и может навредить пациенту, корейские эксперты советуют различать ПВНЛ и ЧВНЛ. Однако стоимость терапии и настойчивое желание пациента продолжить лечение (даже если оно неэффективно) часто перевешивают рекомендации врача или результаты анализа на антитела. По опыту одного из экспертов (Че-Ён Пак) 60–70 % пациентов отказываются от перерывов в лечении, настаивая на продолжении терапии. Поэтому в таких случаях используется препарат инкоА по причине его чистоты и низкого иммуногенного потенциала.
2. Малазийские врачи либо переходят на введение инкоА после подтверждения пациентом возможности оплаты дальнейшего лечения, либо предлагают сделать перерыв в лечении на 1 год. При отсутствии клинического ответа при возобновлении терапии рекомендуется дополнительный перерыв в лечении продолжительностью до 2 лет.
3. Австралийские врачи не имеют возможности проводить анализы на антитела, поэтому тактика ведения пациента определяется его клиническим состоянием. Некоторые врачи (Ниамх Кордафф) переводят пациентов с ЧВНЛ на инкоА, так как, несмотря на непрерывное лечение данным препаратом в течение трех месяцев, титры НАТ снижаются17. В случае пациентов с ПВНЛ перерыв в лечении предпочтительнее, чем замена препарата. В самом начале развития ЧВНЛ или в состоянии, близком к ПВНЛ, обязательно обсуждают с пациентом возможности увеличения дозы и стоимости терапии, а также вопросы снижения эффективности или продолжительности сохранения эффекта. Могут порекомендовать пациенту другой метод лечения (например, микросфокусированный ультразвук).
4. За последнее десятилетие в некоторых регионах Восточной Азии (в частности, в Корее и Гонконге) выросло число процедур коррекции тела, связанных с желанием пациентов сделать голени более стройными и визуально удлинить шею за счет инъекций в соответствующие мышцы.
Несмотря на недавние публикации, посвященные анализам на антитела к БТА (Р. Ванитпхакдидеча/R. Wanitphakdeedecha)13,18, и разработанные некоторыми экспертами собственные тест-системы (И. И. Чао/YY Chao), для дифференциации НАТ от антител, не обладающих нейтрализующей активностью, необходимо улучшить точность или специфичность используемых методов анализа. Важно иметь в виду, что отсутствие клинического ответа может быть, помимо всего прочего, связано с введением недостаточной дозы препарата, например из-за неправильной техники инъекции или неправильного разведения препарата. Анализ на антитела в таких ситуациях бесполезен. Однако если ВНЛ обусловлена именно образованием нейтрализующих антител, то необходима их количественная оценка. Титр антител можно учитывать для прогноза продолжительности перерыва в лечении: чем выше титр, тем более длительный перерыв потребуется. Важно отметить, что переходить на введение высокоочищенных препаратов БТА, не содержащих комплексообразующих белков и других примесей, следует до того, как у пациента появятся признаки резистентности. В сущности, следует рассмотреть возможность применения очищенного препарата с самой низкой иммуногенностью у пациентов, ранее не получавших лечения, чтобы с самого начала снизить риск развития ВНЛ. Как показывает опыт, для лечения ЧВНЛ эксперты чаще переходят на инкоА, тогда как в случае ПВНЛ эксперты чаще рекомендуют перерывы в лечении на 2–2,5 года. Чтобы свести к минимуму риск повторной активации иммунной системы, эксперты рекомендуют возобновлять лечение препаратом БТА, очищенным от лишних бактериальных белков и компонентов19.
Мезотоксин или БТА для внутрикожного введения были расценены как более иммуногенные, чем обычные препараты для внутримышечных инъекций для коррекции мимических морщин. Отчасти это связано с особенностью процедур, в ходе которых вводятся относительно более высокие дозы (до 100 единиц за сеанс). Кроме того, в дерме находится много антигенпрезентирующих дендритных клеток16, играющих ключевую роль в инициации иммунного ответа. Именно они выполняют захват антигена и презентируют его Т-лимфоцитам. Эти физиологические особенности используются, например, в вакцинологии; некоторые вакцины вводятся внутрикожно, чтобы обеспечить более сильный иммунный ответ20. При введении БТА в другие зоны тела, согласно показаниям, используются значительно более высокие дозы (несколько сотен единиц), что увеличивает воздействие на пациента чужеродных белков и риск образования НАТ. Следовательно, в таких ситуациях целесообразно использовать высокоочищенный препарат БТА, содержащий только нейротоксин с молекулярной массой 150 кДа. Курсовое применение таких препаратов сводит к минимуму риск иммуногенности и обеспечивает стойкость результатов лечения и эффективность в долгосрочной перспективе.
Считается, что более новые лекарственные формы токсина от азиатских производителей содержат примеси в большем объеме. Результаты исследований чистоты препаратов БТА4,15 соотносятся с общими представлениями корейских врачей о повышенном риске иммуногенности, связанном с применением препаратов корейского производства. Важно отметить, что некоторые производители БТА могут путать понятия стерильности препарата и чистоты токсина при обсуждении этих вопросов с врачами. Чистоту токсина следует определять как отсутствие лишних бактериальных компонентов, таких как комплексообразующие белки, инактивированный нейротоксин, флагеллин и примеси ДНК15. Согласно проведенному опросу, при сравнении с инкоА, абоА и онаА наиболее часто врачи используют в практике препарат Ботулакс (58,82 %), затем — Медитоксин (32,35 %), Набота (5,88 %) и Иннотокс (2,94 %) (данные не представлены графически). Большинство экспертов сочли, что эти препараты дают сопоставимый эффект мышечного паралича (61,76 %), 20,59 % посчитали, что эти препараты были сильнее, а 17,65 % — что они слабее. Большинство экспертов (73,53 %) также посчитали, что продолжительность действия этих препаратов была короче, в то время как 23,53 % считали, что этот показатель был сопоставим, а 2,94 % указали, что действие этих препаратов сохранялось дольше.
Иммуногенность БТА и ее клинические последствия были изучены в рамках многих исследований5,14,21–24. По сути, БТА — это чужеродный антиген, способный индуцировать образование НАТ25,26, которые ослабляют терапевтическое действие токсина24. Это может привести к частичной неэффективности лечения (в виде снижения интенсивности и (или) продолжительности терапевтического эффекта) или даже к полной неэффективности лечения (отсутствию терапевтического эффекта). В описании одного клинического случая27 было показано постепенное повышение уровня антител наряду с сокращением продолжительности терапевтического эффекта («дрейф» временного интервала между дозами) и потребностью в более высоких дозах для достижения тех же результатов («дрейф» дозы). Большинство доступных на рынке препаратов БТА содержат дополнительные вещества, такие как гемагглютинины (в частности, HA3328), инактивированный нейротоксин1,4, флагеллин29 и фрагменты клостридиальной ДНК30, которые передают сигналы «опасности», связываясь со специфическими рецепторами на дендритных клетках15. Активированные дендритные клетки интернализуют и перерабатывают чужеродные белки, впоследствии представляя элементы чужеродного материала Т-хелперным лимфоцитам, которые активируются и стимулируют созревание В-лимфоцитов в плазматические клетки для выработки антител. Чистый активный нейротоксин с молекулярной массой 150 кДа сам по себе является слабым иммуногеном, не связанным с известными паттерн-распознающими рецепторами или толл-подобными рецепторами на дендритных клетках31. Однако, когда вместе с нейротоксином с молекулярной массой 150 кДа вводятся дополнительные вещества, содержащиеся в препарате, они активируют дендритные клетки, которые могут случайно интернализовать и нейротоксин. После этого активированные дендритные клетки представляют элементы молекулы с массой 150 кДа, активируя Т-хелперы, что приводит к продукции НАТ В-лимфоцитами. В АТОР Ксеомин является единственным коммерчески доступным препаратом нейротоксина, который не содержит комплексообразующих белков и других примесей бактериального происхождения. Поскольку Ксеомин содержит только активный нейротоксин с молекулярной массой 150 кДа, маловероятно, чтобы он подавал сигнал «опасности», вызывающий иммунный ответ, и, следовательно, риск выработки НАТ на фоне применения этого препарата очень низкий. На сегодняшний день у пациентов, ранее не получавших лечения, не наблюдалось ни одного случая ВНЛ вследствие образования НАТ на фоне применения Ксеомина. Поскольку подробное исследование выходит за рамки этой статьи, рекомендуем ознакомиться с недавним обзором32, в котором обсуждается иммуногенность, обусловленная применением препаратов ботулотоксина с комплексообразующими белками или без них, а также клинические и доклинические доказательства этих наблюдений.
Несмотря на то, что чистота токсина — критический фактор риска развития ВНЛ, следует учитывать и другие факторы, в том числе высокую терапевтическую дозу, кумулятивную дозу, короткие интервалы между инъекциями, бустерные инъекции (повторные инъекции) в течение 3 недель после первоначальной инъекции и иммунную реактивность пациента. Во всем мире БТА также используется по многим незарегистрированным эстетическим показаниям, таким как уменьшение мышечного объема33, коррекция формы лица34 и коррекция контуров тела35. На смену низким дозам (до 50 ед.), применяемым обычно в зоне лица, приходят более высокие дозы для коррекции контуров и лифтинга (100 ед. и более), уменьшения объема жевательных мышц и околоушных желез (в Корее и Таиланде), коррекции платизмы, подчеркивания линии челюсти и интрадермального лифтинга лица36. Помимо лица БТА используется в других зонах тела — для уменьшения объема трапециевидной мышцы37 и контурирования плеч38, бедер34 или голеней39. По опыту одного из авторов (Че-Ён Пак), процедуры по уменьшению объема голени проводятся каждые 6 месяцев с применением внутримышечных инъекций, в результате чего кумулятивная доза введенного токсина за 4-летний период достигает приблизительно 640 ед. Однако в случае очень крупных икроножных мышц кумулятивная доза за 3 года составит 2400 ед. ботулинического токсина. Использование таких высоких доз может стать причиной вторичного отсутствия ответа на БТА. Таким образом, в случае снижения или отсутствия клинического ответа на введение БТА, а также в случае укорочения длительности эффекта всегда следует учитывать возможную ВНЛ, связанную с выработкой НАТ.
Более того, нередко предполагаемая ВНЛ на самом деле может быть связана с введением БТА в неправильно подобранных дозах, с использованием неправильной техники или с неправильным хранением, подготовкой препарата, а не с образованием НАТ. Таким образом, в АТОР задача врача состоит не в том, чтобы проводить рутинные анализы на предмет НАТ, а скорее в том, чтобы предпринять все возможные меры для предотвращения нежелательной активации иммунной системы. Для этого с самого начала терапии необходимо применять высокоочищенные препараты БТА, содержащие только действующее вещество с молекулярной массой 150 кДа. Это особенно важно для пациентов, ранее не получавших БТА, планирующих получать высокие дозы за один сеанс или чаще, чем рекомендуется, или проходить лечение в течение длительного периода времени. Кроме того, кумулятивная доза ботулинического токсина, полученная в течение всей жизни, в итоге будет выше у пациентов, начинающих терапию в более молодом возрасте. На практике применение только высокоочищенных препаратов БТА может быть достигнуто за счет пересмотра устаревших представлений об иммуногенности токсина и получения достоверных знаний. Врачам следует выбирать препарат, основываясь на подтвержденных научных данных, и руководствоваться литературными источниками с доказательными данными о чистоте препарата, а также быть в курсе актуальных клинических исследований по иммуногенности препаратов в эстетической медицине. Примечательно, что эксперты расценили выбор высокоочищенного БТА как превентивную стратегию, обеспечивающую возможность длительного применения БТА по терапевтическим или неврологическим показаниям, если это будет необходимо.
ЗАКЛЮЧЕНИЕ
Эксперты из АТОР отмечают увеличение числа пациентов с клинической резистентностью к ботулиническому токсину или развитием ВНЛ вследствие образования НАТ. Эти явления совпали по времени с выводом БТА в более широкую клиническую практику, применением его в более высоких дозах и появлением большего количества коммерчески доступных препаратов БТА. Основываясь на своих личных клинических наблюдениях и опубликованных исследованиях по чистоте токсинов4,15, эксперты пришли к выводу, что в большинстве препаратов в той или иной степени содержатся примеси в виде бактериальных компонентов, способных стимулировать выработку НАТ. Таким образом, для обеспечения долгосрочной эффективности лечения и удовлетворенности пациентов врачам следует избегать применения препаратов, содержащих посторонние компоненты, ввиду повышения риска развития ВНЛ, а также рассмотреть возможность выбора высокоочищенного препарата БТА, чистота которого подтверждается надежными приводимыми в научной литературе доказательствами.
СПИСОК ЛИТЕРАТУРЫ
1. Kerscher M, Wanitphakdeedecha R, Trindade de Almeida A, et al. IncobotulinumtoxinA: a highly purified and precisely manufactured botulinum neurotoxin type A. J Drugs Dermatol. 2019;18:52–57.
2. Jeong S. 4 new botulinum toxins to undergo trials in crowded market. Available at https://www.koreabiomed.com/news/arti- cleView.html?idxno=7021. Published 2020. Accessed September 28, 2020.
3. Lim J. Wrinkle treatment companies vie to fill hole left by Meditoxin. Available at http://www.koreaherald.com/view. php?ud=20200506000924. Published 2020. Accessed September 28, 2020.
4. Frevert J, Ahn KY, Park MY, et al. Comparison of botulinum neu- rotoxin type A formulations in Asia. Clin Cosmet Investig Dermatol. 2018;11:327–331.
5. Torres S, Hamilton M, Sanches E, et al. Neutralizing antibodies to botulinum neurotoxin type A in aesthetic medicine: five case reports. Clin Cosmet Investig Dermatol. 2014;7:11–17.
6. Borodic G. Immunologic resistance after repeated botulinum toxin type A injections for facial rhytides. Ophthalmic Plast Reconstr Surg. 2006;22:239–240.
7. Dressler D, Wohlfahrt K, Meyer-Rogge E, et al. Antibody-induced failure of botulinum toxin A therapy in cosmetic indications. Dermatol Surg. 2010;36(Suppl 4):2182–2187.
8. Dressler D. Clinical features of antibody-induced complete second- ary failure of botulinum toxin therapy. Eur Neurol. 2002;48:26–29.
9. Stengel G, Bee EK. Antibody-induced secondary treatment fail- ure in a patient treated with botulinum toxin type A for glabellar frown lines. Clin Interv Aging.2011;6:281–284.
10. Carruthers A, Kane MA, Flynn TC, et al. The convergence of medicine and neurotoxins: a focus on botulinum toxin type A and its application in aesthetic medicine—a global, evidence- based botulinum toxin consensus education initiative: part I: botulinum toxin in clinical and cosmetic practice. Dermatol Surg. 2013;39(3 Pt 2):493–509.
11. Lee SK. Antibody-induced failure of botulinum toxin type A therapy in a patient with masseteric hypertrophy. Dermatol Surg. 2007;33(1 Spec No.):S105–S110.
12. Stephan F, Habre M, Tomb R. Clinical resistance to three types of botulinum toxin type A in aesthetic medicine. J Cosmet Dermatol. 2014;13:346–348.
13. Srinoulprasert Y, Wanitphakdeedecha R. Antibody-induced bot- ulinum toxin treatment failure: A review and novel management approach. J Cosmet Dermatol. 2020;19:2491–2496.
14. Bellows S, Jankovic J. Immunogenicity associated with botulinum toxin treatment. Toxins (Basel). 2019;11:E491.
15. Park JY, Sunga O, Wanitphakdeedecha R, et al. Neurotoxin impurities: a review of threats to efficacy. Plast Reconstr Surg Glob Open. 2020;8:e2627.
16. Malissen B, Tamoutounour S, Henri S. The origins and functions of dendritic cells and macrophages in the skin. Nat Rev Immunol. 2014;14:417–428.
17. Hefter H, Hartmann C, Kahlen U, et al. Prospective analysis of neutralising antibody titres in secondary non-responders under continuous treatment with a botulinumtoxin type A preparation free of complexing proteins—a single cohort 4-year follow-up study. BMJ Open. 2012;2:e000646.
18. Srinoulprasert Y, Kantaviro W, Nokdhes YN, et al. Development of inhibition ELISA to detect antibody-induced failure of botuli- num toxin a therapy in cosmetic indications. J Immunol Methods. 2019;473:112635.
19. Dressler D, Pan L, Adib Saberi F. Antibody-induced failure of botulinum toxin therapy: re-start with low-antigenicity drugs offers a new treatment opportunity. J Neural Transm (Vienna). 2018;125:1481–1486.
20. Zhang L, Wang W, Wang S. Effect of vaccine administration modality on immunogenicity and efficacy. Expert Rev Vaccines. 2015;14:1509–1523.
21. Brin MF, Comella CL, Jankovic J, et al.; CD-017 BoNTA Study Group. Long-term treatment with botulinum toxin type A in cervical dystonia has low immunogenicity by mouse protection assay. Mov Disord. 2008;23:1353–1360.
22. Jankovic J, Vuong KD, Ahsan J. Comparison of efficacy and immunogenicity of original versus current botulinum toxin in cervical dystonia. Neurology. 2003;60:1186–1188.
23. Naumann M, Boo LM, Ackerman AH, et al. Immunogenicity of botulinum toxins. J Neural Transm (Vienna). 2013;120:275–290.
24. Benecke R. Clinical relevance of botulinum toxin immunogenic- ity. BioDrugs. 2012;26:e1–e9.
25. Schellekens H. Immunogenicity of therapeutic proteins: clinical implications and future prospects. Clin Ther. 2002;24:1720–1740; discussion 1719.
26. Göschel H, Wohlfarth K, Frevert J, et al. Botulinum A toxin ther- apy: neutralizing and nonneutralizing antibodies—therapeutic consequences. Exp Neurol. 1997;147:96–102.
27. Dressler D, Bigalke H. Immunological aspects of botulinum toxin therapy. Expert Rev Neurother. 2017;17:487–494.
28. Bryant AM, Cai S, Singh BR. Comparative immunochemical characteristics of botulinum neurotoxin type A and its associated proteins. Toxicon. 2013;72:126–132.
29. Mizel SB, Bates JT. Flagellin as an adjuvant: cellular mechanisms and potential. J Immunol. 2010;185:5677–5682.
30. Frevert J, Groenewald C. Presence of clostridial DNA in botuli- num toxin products. Toxicon. 2015;93(suppl.):S28–S41.
31. Dey AK, Srivastava IK. Novel adjuvants and delivery systems for enhancing immune responses induced by immunogens. Expert Rev Vaccines. 2011;10:227–251.
32. Carr WW, Jain N, Sublett JW. Immunogenicity of botulinum toxin formulations: potential therapeutic implications. Adv Ther. 2021;38:5046–5064.
33. Kim NH, Park RH, Park JB. Botulinum toxin type A for the treat- ment of hypertrophy of the masseter muscle. Plast Reconstr Surg. 2010;125:1693–1705.
34. Klein FH, Brenner FM, Sato MS, et al. Lower facial remodeling with botulinum toxin type A for the treatment of masseter hyper- trophy. An Bras Dermatol. 2014;89:878–884.
35. Seo K. Body contouring with botulinum toxin. In: Seo KK, ed. Botulinum Toxin for Asians [Ebook]. 1st ed. Singapore: Springer; 2017:141–157.
36. Goldenberg G, Do T, Dong J, Lanoue J. An update on neurotoxin products and administration methods. Available at https://www. mdedge.com/dermatology/article/111411/aesthetic-dermatol- ogy/update-neurotoxin-products-and-administration. Published 2020. Accessed August 2, 2021.
37. Lee JH, Lee KY, Kim JY, et al. Botulinum toxin injection-site selec- tion for a smooth shoulder line: an anatomical study. Biomed Res Int. 2017;2017:3092720.
38. Seo KK, Lee W. Medytoxin/Neuronox. In: Carruthers JCA, ed. Botulinum Toxin. Philadelphia, Pa.: Elsevier; 2012:52–58.
39. Lee HJ, Lee DW, Park YH, et al. Botulinum toxin A for aesthetic contouring of enlarged medial gastrocnemius muscle. Dermatol Surg. 2004;30:867–871; discussion 871.