Т. Полийчук, врач-косметолог, кандидат медицинских наук, доцент
Т. Королькова, врач-дерматовенеролог, косметолог, доктор медицинских наук, профессор, заведующая кафедрой
Кафедра косметологии СЗГМУ им. И.И. Мечникова, Санкт-Петербург, Россия
ВВЕДЕНИЕ
В современной косметологии метод контурной пластики давно завоевал свое прочное место, войдя в тройку наиболее популярных методов неоперативного омоложения лица. В первую очередь это происходит за счет получения быстрых результатов «на кончике иглы», относительной безопасности современных материалов и экономической привлекательности. Тем не менее на протяжении последних лет случаи нежелательных явлений после применения филлеров различного происхождения регистрируются в разных странах, что может коррелировать как с растущей популярностью метода, так и с недостаточной разработкой четких алгоритмов проведения безопасного вмешательства. Сложность
индивидуальной анатомии лица во многом обуславливает отсутствие таких алгоритмов и делает контурную пластику при кажущейся простоте одним из самых рискованных вмешательств в эстетической медицине.
Несмотря на относительно небольшое количество нежелательных явлений (НЯ), они должны быть тщательно проанализированы. Существуют разные классификации НЯ (по времени наступления, этиологии, тяжести проявлений и др.). Кроме того, профиль НЯ зависит от природы дермального наполнителя, техники проведения процедуры, инструментария.
НЕЖЕЛАТЕЛЬНЫЕ ЯВЛЕНИЯ ПОСЛЕ ВВЕДЕНИЯ ФИЛЛЕРОВ
Представляются интересными данные исследования IFS, проведенного в 2003–2012 годах на базе медицинского университета Берлина и посвященного изучению влияния НЯ после контурной пластики на показатели качества жизни пациентов [1]. Целями этого исследования, базирующегося на частичном популяционном анализе, были описание типов и частоты появления побочных реакций, определение профиля безопасности и исследование терапевтических стратегий при возникновении НЯ. Критерии включения в исследование были следующие: пациент должен был быть пролечен филлером и НЯ должно было возникнуть хотя бы в одной из пролеченных зон и длиться по меньшей мере в течение 2 недель. Не рассматривали состояния гиперкоррекции (т.е. исключали врачебный фактор). В качестве НЯ учитывали эритему, формирование узлов, абсцесс, боль, изменение окраски кожи, которые оценивали с использованием стандартно
го атласа клинических симптомов. Интенсивность реакций оценивали по 3-бальной шкале от одного (легкая) до трех (тяжелая).
Индекс качества жизни (ИКЖ) становится все более важным в последние десятилетия. В 1994 году Finlay и Khan для оценки влияния кожных заболеваний на качество жизни предложили так называемый дерматологический индекс качества жизни (ДИКЖ). Он представлен стандартными, подтвержденными, понятными и простыми критериями и используется как в клинических испытаниях, так и в ежедневной практике лечения таких дерматозов, как псориаз, акне, экзема, витилиго и др. До этого исследования, по мнению авторов, не было данных о том, как влияют НЯ после контурной пластики на показатели качества жизни.
Начиная с 2008 года пациентов, принявших учаcтие в исследовании IFS, просили заполнить отредактированный опросник ДИКЖ. Каждый вопрос подразумевал выбор одного из ответов: «нет», «немного», «значительно» и «очень значимо», что соответствовало баллам от 0 до 3 (ответ «нет» оценивался как 0 баллов). ДИКЖ оценивали как сумму баллов, полученных при ответе на каждый вопрос. Максимальный результат в 30 баллов означал очень сильное влияние, минимальный (0 баллов) – отсутствие влияния. Другими словами, чем выше балл, тем сильнее НЯ влияет на качество жизни.
Проведен анализ НЯ у 104 пациентов, из которых 88,5% (92 человека) – женщины, 11,5% (12 человек) – мужчины. Средний возраст – 49,2 года; около 40% опрошенных были в возрасте от 50 до 59 лет.
Половина (50%) пациентов получили инъекции биодеградирующих филлеров (основная группа), 40,4% – перманентных (1-я группа сравнения), остальным проведено комбинированное лечение (2-я группа сравнения). В целом этим 104 пациентам было выполнено 260 процедур контурной пластики, из них 34,6% пациентов получили одну процедуру, 25,9% – две; 16,4% – три; 15,4% – четыре процедуры. У 7,7% опрошенных контурную пластику проводили пять и более раз. Применяли 28 разных филлеров.
Варианты и распространенность нежелательных явлений после введения филлеров
Всего было описано 614 побочных реакций, или НЯ. У одного из пациентов в одном и том же месте трижды появлялись отек, зуд и покраснение, что было подсчитано как три НЯ. Как правило, побочные реакции были представлены:
– «узлами» (например, гранулемой инородного тела или уплотнением (инфильтратом) (29,6%, или n=182) с последующим развитием отека (19,5%, или n=120);
– эритемой и воспалением (16%, или n=98);
– болью в зоне инъекции (12,2%, или n=72);
– изменением цвета кожи (10,7%, или n=66);
– абсцессом (5,2%, или n= 32);
– зудом (4,7%, или n=29);
– другими НЯ (1,95%, или n=12).
Сосудистых осложнений не было.
Достоверная информация была собрана о 595 случаях побочных реакций из 614. Большинство из них развились в области носогубных складок (23,4%, или n=126), далее по убывающей – на верхней губе (15,2%, или n=82), щеках (11,9%, или n=64), глабелле (8,2%, или n=44), в углах рта (6,3%, или n=34) и на подбородке (5,8%, или n=31). Причем после применения биодеградирующих филлеров набольшее количество НЯ были локализованы в области носогубных складок и верхней губы, а после применения перманентных – не только там, но еще и в области щек, глабеллы, подбородка, лба и углов рта.
По степени интенсивности 225 НЯ пациенты оценивали как мягкие (37,6%), 217 – как средней степени выраженности (36,2%) и 157 – как тяжелые (26,2%). Легкие НЯ были представлены уплотнениями (21,3%) с последующим изменением цвета кожи (15,1%) и развитием воспалительной эритемы в зоне введения препарата (14,2%). Реакции средней степени выраженности – инфильтратами (35,5%), отеком (17,1%) и воспалительной эритемой (16,1%). Среди тяжелых НЯ преобладали «узлы» (33,1%) и отеки (также 33,1%).
Влияние побочных реакций на дерматологический индекс качества жизни
ДИКЖ суммарно оценивает влияние НЯ на такие характеристики, как уверенность в себе, влияние на различные сферы жизнедеятельности (спорт, работу или учебу, досуг, сексуальную активность, взаимоотношения с друзьями, имидж и др.).
Анализ показал, что 25% пациентов (n=26) сообщили об отсутствии влияния процедур на ДИКЖ (0–1 балла); 21,2% (n=22) – о незначительном их влиянии (ДИКЖ=2–5 баллов); 16,3% (n=17) оценивали их влияние как среднее (ДИКЖ=6–10 баллов); 24% (n=25) сообщили о существенном влиянии НЯ на ДИКЖ (11–20 баллов) и 13,4% (n=14) оценили их влияние как очень большое (ДИКЖ=21–30 баллов). Причем в группе участников, инъецированных перманентными филлерами, 45,2% пациентов отмечали сильное или очень сильное влияние НЯ на индекс качества жизни, тогда как в группе инъецированных биодеградирующими препаратами этот показатель был ниже (34,6%). Умеренное влияние НЯ на ДИКЖ в основной группе оценили в среднем в 8,9 балла, а пациенты 1-й группы сравнения – в 10,5 балла. Интересно, что наибольшее недовольство у пациентов вызывали сложности маскировки дефектов, ограничение досуга, снижение уверенности в себе (средняя оценка 1,5 балла). В то же время побочные эффекты практически не влияли на работу, взаимоотношения с друзьями и родственниками и жизнелюбие (средняя оценка 0,4 балла).
Как уже было сказано, участникам исследования вводили как биодеградирующие, так и небиодеградирующие (перманентные) филлеры. Среди перманентных филлеров чаще всего применяли «Дермалайф» (у 17 пациентов) и «Аквамид». Реже вводили силикон, полиакриламид, «Артеколл», «Биоалкамид» (в каждом случае у 4 пациентов). Среди биодеградирующих наполнителей по частоте применения лидировал «Нью-филл»/«Скульптра» (у 15 человек), «Рестилайн»
(у 12), и гораздо реже «Белотеро», «Дермиаль», «Эволанс», «Гиакорп», «Гилаформ», «Ювидерм», коллаген, «Матридур», «Ревидерм», «Теосиаль», «Вариодерм» (в среднем каждый у 1–3 человек). Это необходимо учитывать при оценке конечных результатов данного исследования.
Для подведения итогов исследования IFS все пациенты были разделены на две группы: G1 – лица, у которых НЯ не повлияли или повлияли незначительно на качество жизни, и G2 – лица, у которых НЯ повлияли значительно и даже очень
сильно. В группу G1 вошел 21 пациент (20,2%), из них 10 человек получили инъекции биодеградирующих препаратов, 7 – перманентных и 4 – комбинированное лечение. Группу G2 составили 14 пациентов (13,4%), большинство из которых (57,1%) были пролечены перманентными филлерами и 42,9% – биодеградирующими. ДИКЖ в этой группе составил 21–30 баллов. Также эти группы отличались по локализации НЯ: в группе G1 примерно ¾ всех побочных реакций были сосредоточены в нижней трети лица, тогда как в группе G2 значительная их часть (44,8%) локализовалась в средней трети лица.
Большая часть НЯ в группе G1 поддавалась терапии: о полном излечении без последствий сообщили 28,5% пациентов. К сожалению, в группе G2 не было ни одного пациента, кто бы излечился полностью. Значительная часть НЯ в группе G2 продолжались в течение всего времени проведения исследования, и даже наблюдались случаи ухудшения (19,1%). Конечно, имеет значение время проведения анкетирования, так как если на момент опроса НЯ уже были излечены, то пациенты воспринимали их как более легкие, незначительные, в противоположность текущим НЯ, которые еще не разрешились. Положительно на оценку ДИКЖ также влияли способность препарата биодеградировать и удаленность локализации НЯ от глаз.
Кроме того, в этом исследовании была проведена корреляция между показателями ДИКЖ у пациентов с НЯ после контурной пластики и у пациентов с наиболее распространенными дерматозами. Интересно, что уровень ДИКЖ у пациентов с НЯ после введения перманентных филлеров был близок к таковому у пациентов с атопическим дерматитом (10,5 и 12,5 балла соответственно), а у пациентов с НЯ на введение биодеградирующих препаратов – к уровню ДИКЖ у пациентов с псориазом (по 8,9 балла).
Сосудистые осложнения после контурной пластики
К сожалению, в данной работе не обсуждали пути профилактики развития НЯ после контурной пластики и, как уже говорилось выше, среди описанных НЯ не было сосудистых осложнений. Однако сложность и многообразие анатомических вариантов постоянно предоставляют новые данные, что влечет за собой к изменению или расширению протокола выполнения процедур. Для примера поговорим о кровоснабжении лобной области.
Область лба снабжают кровью две артерии, выходящие из орбиты в области глабеллы, – это парные надглазничные и надблоковые артерии (из бассейна внутренней сонной артерии), а также парные поверхностные височные артерии, лобные ее ветви, исходящие из бассейна наружной сонной артерии. Надглазничные и надблоковые артерии – ветви глазной артерии, которая, в свою очередь, сообщается с артерией сетчатки. Поэтому инъекции филлеров иглой в области переносицы считаются опасными, поскольку чреваты развитием слепоты во время процедуры [2].
Выйдя по переднему краю орбиты в область лобной кости, надглазничные и надблоковые артерии проходят сквозь апоневроз и поднимаются кверху и кпереди, прободая глабеллярный мышечный комплекс, и далее, распадаясь на более мелкие ветви, идут по передней поверхности лобных мышц под поверхностной фасцией. Поэтому коррекция иглой поперечных морщин лба на 1,5 см над надбровными дугами также чревата риском внутрисосудистого введения филлера. Здесь инъекции следует проводить супрапериостально, хотя необходимо помнить о том, что у некоторых людей описаны глубокие надкостничные ветки надглазничных и надблоковых артерий [2].
Что касается поверхностных височных артерий, то между их лобными ветвями и надблоковой и надглазничными артериями иногда появляются анастомозы. Поэтому существует риск их повреждения и развития слепоты, даже если инъекции проводят не в области глабеллы, а на расстоянии от нее. При случайном попадании иглы в сосуд направление продвижения фрагмента филлера определяется несколькими факторами и зависит от систолического давления, диаметра сосуда, вязкости препарата и др. Филлер может распространяться как дистально, так и проксимально, и даже, пересекая срединную линию по коллатералям, переходить на другую сторону лица. Поэтому признаки сосудистой катастрофы не всегда очевидны на процедуре и могут развиваться отсроченно.
В связи с этим с целью уменьшить риск внутрисосудистой эмболизации многие практикующие специалисты используют гибкие тупоконечные канюли. Но, по мнению T. Tansatit и соавт. [3], канюли не гарантируют полной безопасности при проведении инъекций. На кадаверном материале они продемонстрировали возможность перфорации канюлей 25 G стенки лобной ветви височной артерии диаметром 1,2–1,5 мм. Такую вероятность демонстрирует рисунок 1.
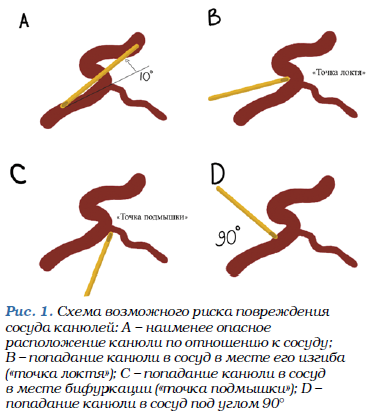
По мнению авторов вышеупомянутой статьи, сосуды крупного диаметра повредить легче, чем сосуды малого диаметра [3]. Авторы рекомендуют проводить инъекции, избегая проекции крупных сосудов.
На примере лобной зоны мы рассмотрели разнообразие рекомендаций по проведению инъекций, исходя из пополняющихся знаний об индивидуальной анатомии лица. Тем не менее тема профилактики наиболее грозных НЯ в контурной пластике остается актуальной и требует дальнейшей разработки.
ЗАКЛЮЧЕНИЕ
Проведенный анализ видов и частоты встречаемости различных осложнений после инъекционной контурной пластики показал, что основная масса нежелательных явлений носит плановый характер и разрешается практически без врачебного вмешательства. В то же время, чтобы максимально снизить риск возникновения серьезных осложнений, врачу следует по возможности применять биодеградирующие филлеры, строго соблюдать все требования и протоколы выполнения процедуры коррекции, тщательно изучать анатомию лицевой области, включая новые данные об индивидуальном анатомическом строении.
ЛИТЕРАТУРА
1. Duker D, Erdmann R, Hartmann V, et al. The impact of adverse reactions to injectable filler substances on quality of life: results from the Berlin Injectable Filler Safety (IFS)-study. // J Eur Acad Dermatol Venerol, 2016;30:1013 –1020.
2. Инъекционные филлеры: моделирование и контурная пластика лица. Под ред. А. Дерека, А. Свифта. Пер. с англ. под ред. Т.Н. Корольковой. – Москва: ГОЭТАР-Медиа, 2022.
3. Tansatit T, Apinuntrum P, Phetudom T, et al. A Dark Side of the Cannula Injections: How Arterial Wall Perforations and Emboli Occur. // Aesth Plast Surg, 2017;41(1):221–227.
