Автор: Казаков Сергей Павлович, врач-косметолог
За всю историю существования биоревитализации сменилось уже несколько поколений, представители которых предъявляют все новые и новые требования к оказанию косметологической помощи, стимулируя нас к развитию и новым разработкам. Характерной чертой запросов пациентов последних лет стала нацеленность на малую травматичность, низкий риск реабилитационных последствий, но при этом высокую, если не сказать большую, эффективность медицинских косметологических манипуляций.
Какие же изменения коснулись метода? Понимая свойства гиалуроновой кислоты как активного участника обменных процессов в коже, производители разработали новые составы биоревитализантов, которые способствовали повышению их эффективности и расширению спектра показаний к применению. В арсенале косметологов появились многокомпонентные препараты, содержащие метаболический субстрат из витаминов, аминокислот, микроэлементов, пептидов, факторов роста и пр.
Учитывая способность эндогенной и экзогенной гиалуроновой кислоты быстро расщепляться под действием собственных ферментативных систем человеческого организма, еще одним направлением поиска стало изучение дополнительных веществ, которые могли бы затормозить процессы быстрой биодеградации основного действующего вещества и продлить его эффективное действие после имплантации в кожу. Таким образом, появились препараты гиалуроновой кислоты, стабилизированные маннитолом, глицеролом, сахарами, эфирами и металлами. Но и практикующие специалисты не остались в стороне и разработали новые приемы техник, например, инъекции по биоэстетическим и биоактивным точкам, преследуя цель снижения травматизации и сокращения времени самой процедуры без ущерба для конечного эффекта. Вместе с этим родились и новые термины, такие как биорепарация, биореструктуризация, биостимуляция и прочие, зачастую преследующие маркетинговые цели.
В потоке волны изысканий и инноваций разработчики и производители инъекционных косметологических препаратов решились на очень интересный шаг – использовать метод пегилирования веществ, который давно и эффективно применяется в фармацевтике и медицине. И вот совсем недавно привычный арсенал врача-косметолога пополнился таким продуктом.
Но прежде хотелось бы пояснить суть технологии пегилирования.
Под пегилированием понимают ковалентную модификацию различных веществ фрагментами полиэтиленгликоля для улучшения определенных их свойств. И здесь возникает совершенно справедливый вопрос о безопасности самого полиэтиленгликоля для организма человека. И, к счастью, ответ на этот вопрос найден в исследованиях, проводившихся с 1970 года и продолжающихся по сегодняшний день.
Полиэтиленгликоль (ПЭГ, макрогол) представляет собой полимер, растворимый во множестве органических растворителей и хорошо растворимый в воде. В водных растворах ПЭГ является типичным неионным полимером, для которого характерна способность к образованию различного рода комплексов с некоторыми веществами полимерной и неполимерной природы. Особенности молекулы ПЭГ и расположения в ней функциональных химических групп при взаимодействии с другими веществами, позволяют ему формировать различные комплексы, конъюгаты и надмолекулярные структуры. Высокое содержание атомов кислорода в макромолекулах ПЭГ позволяет им связываться с несколькими молекулами воды. Подобный эффект влечет за собой формирование «водного облака» вокруг модифицированных молекул, благодаря чему значительно повышается их гидродинамический радиус. Именно эти свойства стали ключевыми при выборе этого полимера как безопасной системы для доставки лекарственных веществ с улучшенными свойствами. В фармакологии встречаются такие пегилированные молекулы, как белки, пептиды, ферменты и др., а также ПЭГ-липосомы и наночастицы. Полиэтиленгликоль обладает высокой биосовместимостью, низкой иммуногенностью и антигенностью. По данным международной энциклопедии токсикологии, ПЭГ относится к веществам, не обладающим токсичностью и канцерогенностью. ПЭГ инертен для организма и выводится в неизмененном виде через почки.
Смысл пегилированных систем, применяемых в фармакологии, сводится к замедлению высвобождения активных молекул, повышению времени циркуляции ЛВ в крови, повышению биодоступности и снижению общей токсичности основного действующего вещества ЛС.
Первое упоминание об использовании метода пегилирования в области доставки лекарственных веществ датируется 1977 годом, когда Davis и Abuchowski описали процесс присоединения ПЭГ к бычьему сывороточному альбумину. В 1990 году FDA утвердило первый модифицированный белковый продукт – Adagen®, представляющий собой пегилированный фермент аденозиндеаминазы, направленный на лечение тяжелых форм вируса иммунодефицита. Сегодня пегилированные лекарственные средства применяются в таких сложных областях медицины, как онкология, онкогематология, иммунология и пр.
Таким образом, накопленный опыт применения полиэтиленгликоля в медицине и значительное количество исследований доказывают его безопасность и эффективность.
В составах инъекционных косметологических препаратов полиэтиленгликоль стал использоваться сравнительно недавно. И одним из первых, но единственным в своем роде, стал скинбустер-префиллер Repart PG, выпускаемый российской фармацевтической компанией ИНГАЛ.
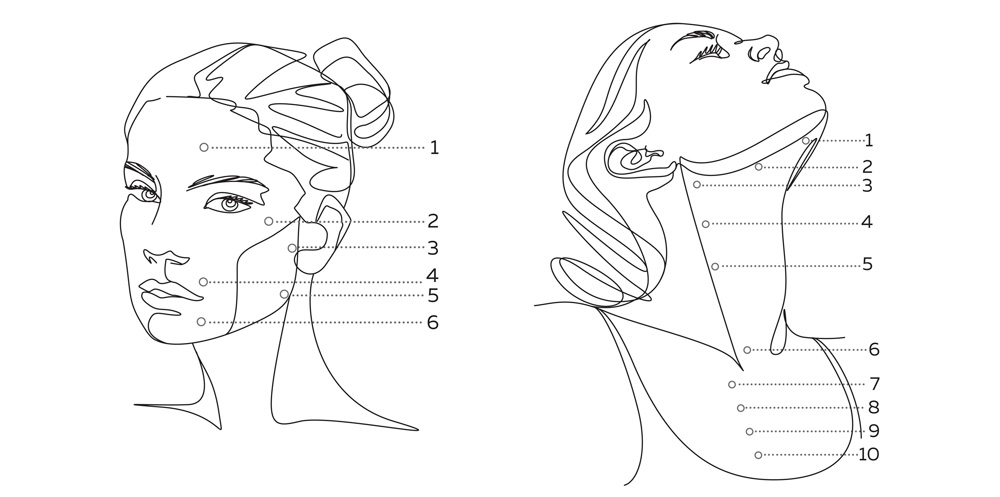
Опираясь на длительный мировой опыт применения полиэтиленгликоля в фармакологии и медицины, сотрудники научно-производственного комплекса ИНГАЛ разработали усовершенствованный биоревитализант или, как принято называть такие препараты в косметологии, – скинбустер. При взаимодействии с гиалуроновой кислотой ПЭГ выступает в качестве легкого сшивающего агента, образуя систему ПЭГ-гиалуронат, устойчивую по отношению к собственным ферментативным системам. Помимо этого, ПЭГ сорбирует на себе гиалуронидазы дермы и замедляет их активную работу. Естественное расщепление такого комбинированного гидрогеля после имплантации в кожу составляет порядка 30 дней, что значительно дольше в сравнении с классическими биоревитализантами, в связи с чем эффективное действие самой гиалуроновой кислоты увеличивается. А это позволяет сократить стандартный курс процедур до 1–2 сеансов. Физико-химические свойства препарата Repart PG таковы, что позволяют применять его по биоэстетическим точкам (рис. 1), сокращая время самого сеанса до 10 минут и снижая риски краткосрочных нежелательных явлений. Repart PG отвечает принципам социальной сохранности косметологических процедур и может выступать в качестве процедуры «обеденного перерыва» без видимых последствий инъекционных вмешательств.
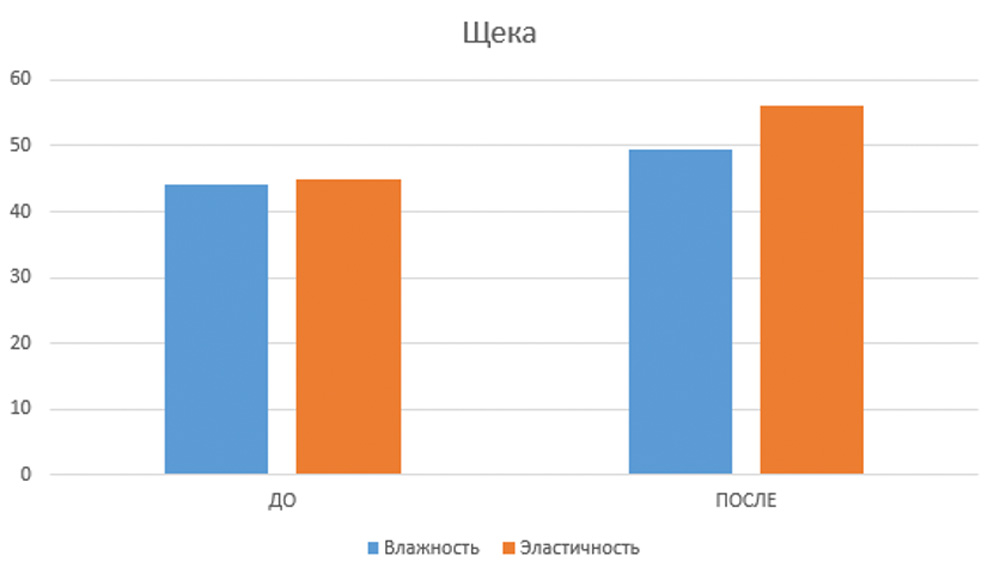
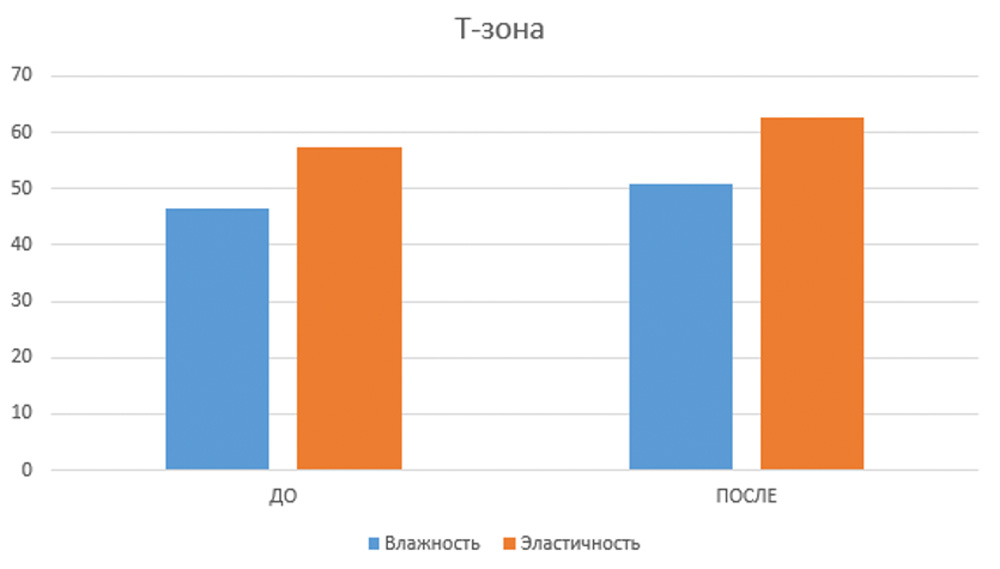
Эффективность и безопасность применения доказана исследованиями, проведенными на базе Школы профессора Юцковской. В испытаниях приняли участие 39 добровольцев, у которых были изучены количественные изменения по показателям увлажненности и эластичности кожи (аппарат диагностики кожи Multi Skin Test Center MC 1000) в результате двухкратной имплантации Repart PG по биоэстетическим точкам с интервалом в 21 день. Визуальные изменения оценивались с помощью 3D-фотодиагностики на аппарате LifeViz Quantificare. У всех испытуемых отмечались визуальные и диагностические улучшения состояния кожного покрова лица. В ходе исследования были получены следующие данные: показатели увлажненности в среднем по группе повысились на 5 пунктов, показатели эластичности – на 6–11 пунктов (рис. 2а, 2б).
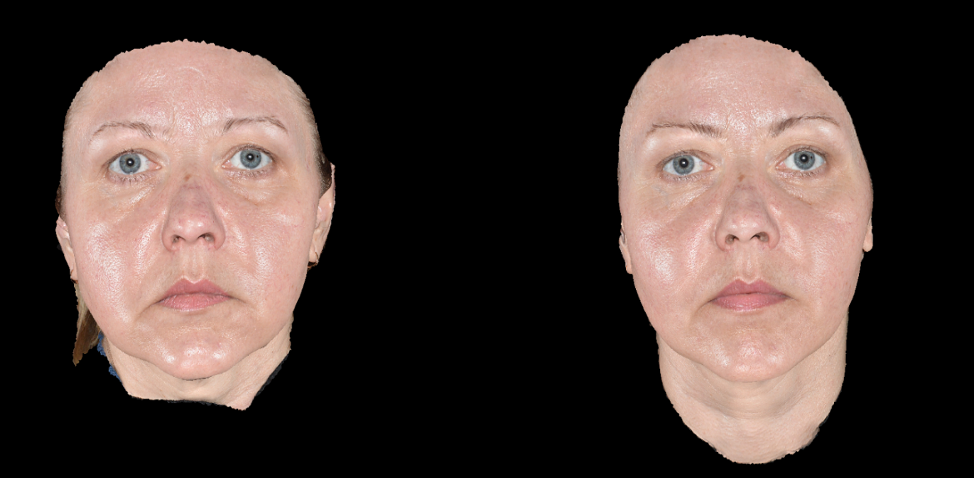
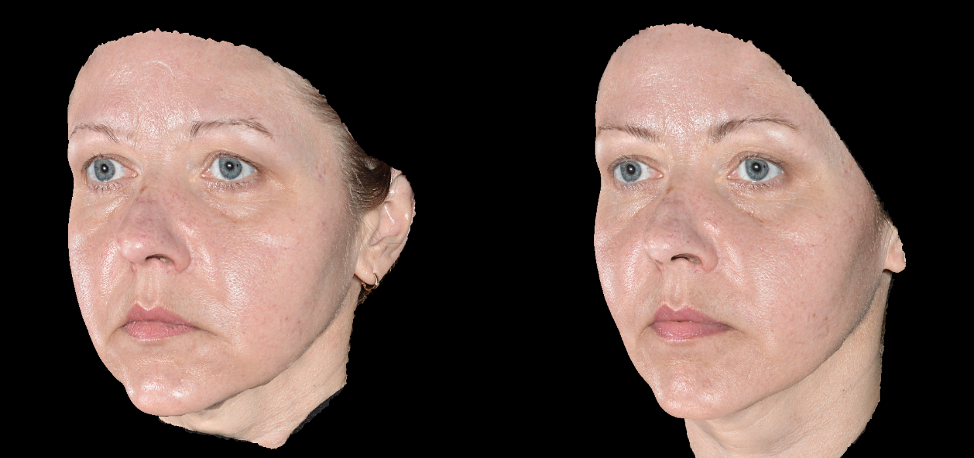
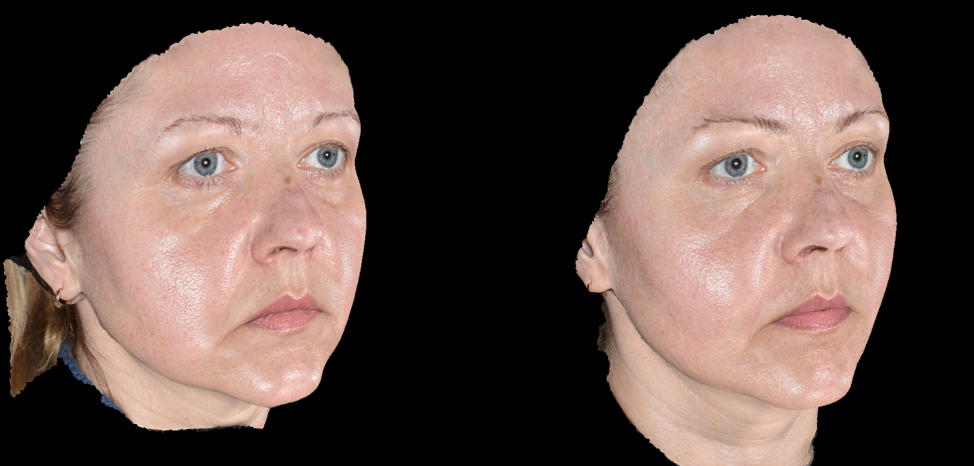
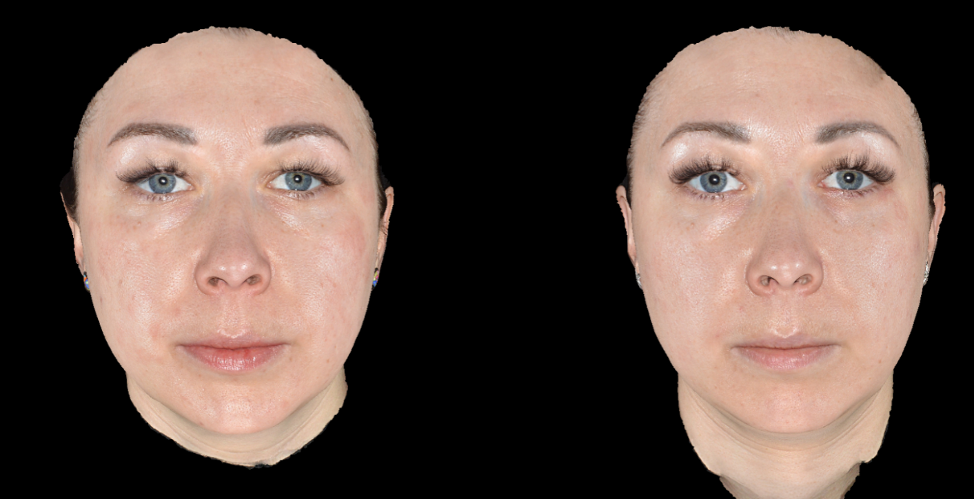
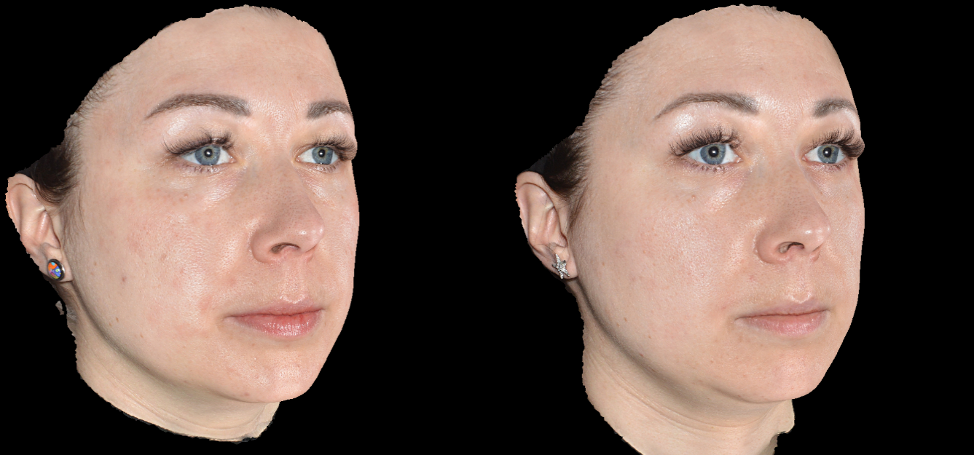
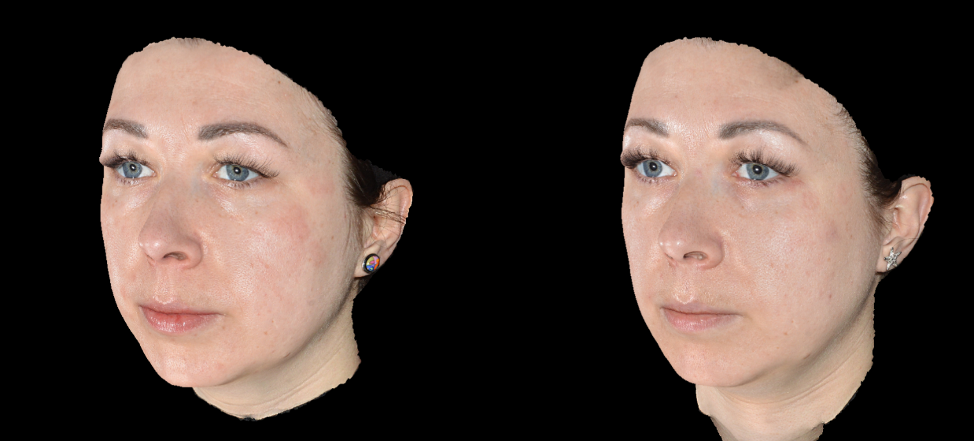
В течение клинических испытаний препаратов не наблюдалось каких-либо осложнений в виде аллергических реакций и других нежелательных явлений. Реабилитационный период составил в среднем от 1 до 5 дней, в течение которых наблюдались единичные экхимозы в местах введения иглы, гиперемия в местах инъекций (сохранялась сутки), папулы в местах введения препарата.
Выводы
Современное развитие косметологии невозможно без внедрения наукоемких технологий, доказанных методов, научного подхода в изучении эффективности и безопасности применяемых методик.
Repart PG представляет собой препарат с уникальными свойствами, применение которого позволяет сократить время процедуры до 10 минут, а количество сеансов до 1–2, повысить комфорт пациента во время имплантации препарата, снизить риск нежелательных явлений и значительно повысить эффективность метода. Repart PG полностью отвечает требованиям времени, запросам и ожиданиям современного пациента.
Источники:
- И.Г. Никитин, И.Е. Байкова, Л.М. Гогова //Лечебное дело. Клиническая фармакология. № 4. 2005. с. 18
- Dr. Hans Lautenschläger // Kosmetische Praxis, 2009, рр. 12-15.
- Porfiryeva, N. N., Moustafine, R. I. and Khutoryanskiy, V. V. (2020) // PEGylated systems in pharmaceutics. Polymer Science Series C, 61 (1). pp. 9-10.
- И.А. Пучков, Д.И. Баирамашвили, В.И. Швец // Вестник МИТХТ, 2014, т. 9, No 2.
- Abuchowski A., McCoy J.R., Palczuk N.C., van Es T., Davis F.F. // J. Biol. Chem. 1977. V. 252. No 11. P. 3582–3586.
- Weissig V., Pettinger T.K., Murdock N. // Int. J. Nanomedicine. 2014. V. 9. P. 4357–4373.

