СПОСОБ ЛЕЧЕНИЯ НЕГАТИВНЫХ ПОСЛЕДСТВИЙ КОНТУРНОЙ ПЛАСТИКИ ЛИЦА ГЕЛЯМИ НА ОСНОВЕ ГИАЛУРОНОВОЙ КИСЛОТЫ
Бондаренко Игорь Николаевич, к.м.н., стоматологическая, косметологическая клиники «Шаритэ», генеральный директор, Краснодар
Матишев Андрей Алексеевич, заместитель директора по научной работе многопрофильной клиники «Центр лазерной медицины», Краснодар
Актуальность проблемы обусловлена популяризацией косметологии, увеличением количества процедур контурной пластики, применением гелей на основе гиалуроновой кислоты в «запрещенных» зонах лица, что, в свою очередь, привело к резкому учащению случаев осложнений контурной пластики, нежелательных эффектов и гиперкоррекции. Наличие на рынке большого количества низкокачественного товара способствует тому, что в зонах введения гелей формируются очаги острого и хронического воспаления, требующие как хирургических, так и иных методов удаления геля [1].
Для коррекции нежелательных последствий контурной пластики гелями на основе гиалуроновой кислоты предлагают использовать различные препараты, действующим веществом которых является гиалуронидаза. Рекомендуется инъецировать препараты с гиалуронидазной активностью в зону дефекта [2]. Причем у подавляющего большинства существующих на сегодняшний день на рынке препаратов, действующим веществом которых является гиалуронидаза, не прописано в инструкциях применение в косметологии. При этом отсутствуют какие-либо рекомендации к каждому из препаратов по дозам, кратности введения, объему вводимого препарата. Также нет четких протоколов введения препарата:
на какую глубину, каким именно способом. Таким образом, специалисты вводят препараты с гиалуронидазой бесконтрольно, практически вслепую, в толщу тканей лица, где предположительно находится гель, без учета анатомических
особенностей пациента и четкого определения локализации филлера, его формы, размеров, топографии относительно иных структур лица. При таком введении препаратов присутствует высокий риск повреждения находящихся в тканях сосудов, нервов и других структур обрабатываемой зоны, а также вероятность введения гиалуронидазы в просвет сосуда или в нерв, минуя сам гель. В зоне интервенции формируется воспалительная реакция окружающих тканей, сопровождающаяся отеком и болью.
По результатам наших наблюдений, недостатками лечения нежелательных последствий контурной пластики гелями на основе гиалуроновой кислоты путем введения в зону коррекции препаратов гиалуронидазы является отсутствие выраженного клинического эффекта и большое количество побочных явлений от проводимой терапии. К ним можно причислить острые отеки в зоне введения, длительно сохраняющуюся пастозность окружающих тканей, риск аллергических реакций, болезненность при введении.
Отсутствие стандартов диагностики, четких схем, инструкций и рекомендаций по лечению пациентов в случаях гиперкоррекции и отеков послужили основанием поиска эффективных и безопасных способов диагностики и коррекции негативных последствий контурной пластики гелями на основе гиалуроновой кислоты.
Альтернативным методом является предлагаемая нами технология, аналогичная воздействию на гипертрофические рубцы фонофорезом с однопроцентной гидрокортизоновой мазью, когда одномоментно идет сочетание механической энергии ультразвуковой волны и химического состава вводимого лекарственного вещества в очаг поражения [3, 4].
Цель и задачи
Цель исследования: разработать алгоритм диагностики и лечения нежелательных последствий контурной пластики лица гелями на основе гиалуроновой кислоты.
Задачи:
1) внедрить в практику врача-косметолога ультразвуковую диагностику (УЗД) осложнений контурной пластики;
2) найти ультразвуковые признаки (УЗ-признаки), характерные для дифференциальной диагностики различных патологических состояний;
3) найти альтернативный способ коррекции осложнений контурной пластики;
4) повысить точность введения лекарственного препарата непосредственно в зону филлера;
5) свести к минимуму риски аллергических и воспалительных реакций при лечении нежелательных последствий контурной пластики;
6) обеспечить безболезненность процедуры коррекции нежелательных результатов контурной пластики.
Материалы и методы
Предлагаемый метод апробирован на 20 пациентах. Группа включала женщин в возрасте от 25 до 44 лет.
В структуре жалоб фигурировали:
• неудовлетворенность эстетическим результатом – 100%;
• гиперкоррекция – 75%;
• асимметрия – 60%;
• отечность в зоне введения – 50%.
Наиболее часто встречающимися зонами коррекции были: носослезные борозды – 50%, губы – 30%, область скул – 10%, подбородок – 10%.
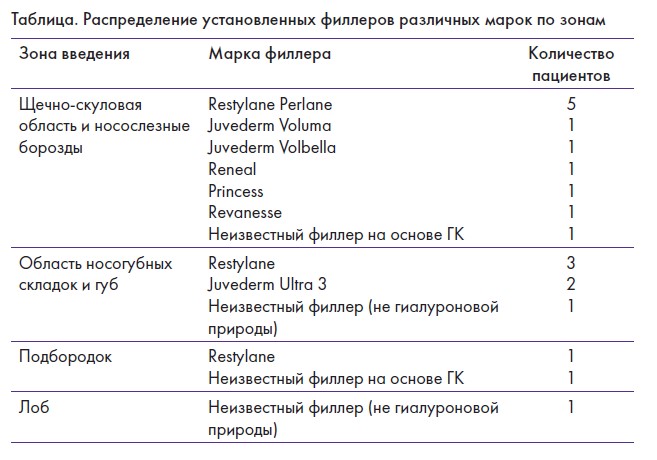
При сборе анамнеза, со слов пациентов, мы выявили следующее распределение установленных филлеров различных марок по зонам (табл.).
После сбора анамнеза проводили осмотр зоны поражения, пальпацию, затем – ультразвуковое исследование на аппарате MyLab Twice (производитель Esaote, Италия).
Четырем пациентам (20%) первичное ультразвуковое исследование проводили после введения препаратов, содержащих гиалуронидазу. У одной из четырех пациенток в анамнезе – многократные инъекции в губы различными филлерами с последующей коррекцией формы препаратами гиалуронидазы. Последняя коррекция асимметрии до поступления к нам в клинику проводилась одномоментным введением 6000 ЕД препарата «Лонгидаза» (двух флаконов в зону губ; клинический пример описан ниже). Трое пациентов поступили с клиникой отека лица и периорбитальной зоны. В одном случае УЗИ проводилось на 14-й день после последнего введения препаратов гиалуронидазы (всего у пациентки было
11-кратное введение препаратов гиалуронидазы). Во втором случае УЗИ осуществлялось на 7-й день и в динамике на 49-й день после последней инъекции гиалуронидазы (всего было восемь инъекций). И в третьем случае УЗИ было проведено до введения препарата «Лонгидаза», а также в динамике после двукратного ежедневного введения препарата по 500 ЕД с каждой стороны, суммарно 2000 ЕД за два дня.
Диагностика. Во время ультразвукового исследования производили поиск подкожных фрагментов геля, четко определяли их локализацию относительно анатомических структур лицевого скелета и глубины залегания от эпидермального слоя кожи лица, устанавливали продольные и поперечные размеры локусов филлера, отмечали взаимоотношения анатомических структур (сосудов, мышц лица, нервных стволов разной степени ветвления, фиброзных образований) и болюсов
филлера. Также определяли структуру окружающих тканей: повышенную пастозность, избыточное фиброзирование, прочие особенности, если таковые имелись, например, наличие имплантатов негиалуроновой природы или изменение скоростных показателей кровотока в сосудах лицевого скелета в случае контакта с ними геля.
Лечение. После этого приступали к лечению, которое осуществлялось в два этапа. На первом этапе в зависимости от клинической картины назначали курс фонофореза с однопроцентной гидрокортизоновой мазью в количестве 6–10 процедур ежедневно с последующим контрольным УЗИ зон воздействия, оценкой динамики уменьшения размеров геля через три недели. После этого у пациентов с филлерами гиалуроновой природы уменьшался отек окружающих тканей, гель биодеградировал: из анэхогенных и гипоэхогенных болюсов с четкими и достаточно ровными контурами до лечения приобретал вид неоднородных по структуре локусов с признаками фиброзирования в виде гиперэхогенных нежных тяжей и явлениями фрагментации данных болюсов.
Затем на оставшийся фрагментированный гель диаметром более 3 мм воздействовали вторым этапом лечения. Под ультразвуковым контролем непосредственно в фокус филлера (отклонение кончика иглы при ультразвуковом наведении не превышало 1 мм), избегая травматизации прилегающих сосудов и нервов, вводили препарат «Лонгидаза» с последующим повторным УЗ-контролем через две недели после введения. Для этого обрабатывали антисептиком кожные покровы
места инъекции, наносили стерильный ультразвуковой гель. Ультразвуковую навигацию выполняли на аппарате линейным датчиком с частотой сканирования 15–18 МГц в режиме small parts probe. Выбирали оптимальную трассу проведения иглы в гель, учитывая положение сосудов, нервов и иных анатомических структур с целью исключения травматизации. При этом использовали как режим серой шкалы, так и режим доплеровского и энергетического картирования, что позволяло получать более качественное изображение и повышало точность и безопасность введения препарата. Инъекцию препарата «Лонгидаза» осуществляли инсулиновым шприцем с несъемной иглой, доза 75–500 международных единиц (МЕ) на один фрагмент геля (болюс) в зависимости от фактического объема болюса, который позволяет вычислить стандартная программа ультразвукового аппарата.
Такое точечное введение препарата «Лонгидаза» описанным способом под УЗ-контролем позволяет минимизировать риски повреждения прилежащих сосудов и нервов, доставить адресно препарат, уменьшив его дозу и объем. Описанный способ лечения был применен к пациентам с локализацией геля в различных зонах мягких тканей лица.
Результаты и обсуждение ультразвукового исследования и последующего лечения
В группе обследованных пациентов, которым вводили филлер на основе гиалуроновой кислоты, по зонам гель распределялся следующим образом (см. табл.): 10 человек (50%) – носослезная борозда, 6 человек (30%) – инфраорбитальная
область (fossa canina), 5 человек (25%) – область скуловой кости, 6 человек (30%) – область губ и носогубных складок, 2 человека (10%) – область подбородка. В 5 случаях (25%) гель прилегал к сосудам, в 12 (60%) – выявлен фиброз. В двух случаях были инъецированы препараты не гиалуроновой природы.
При УЗИ филлеры на основе ГК определялись в виде четких анэхогенных и гипоэхогенных локусов различного диаметра от 3 до 15 мм. По результатам проведенной УЗ-диагностики с учетом анамнеза получены следующие, приводимые
ниже данные.
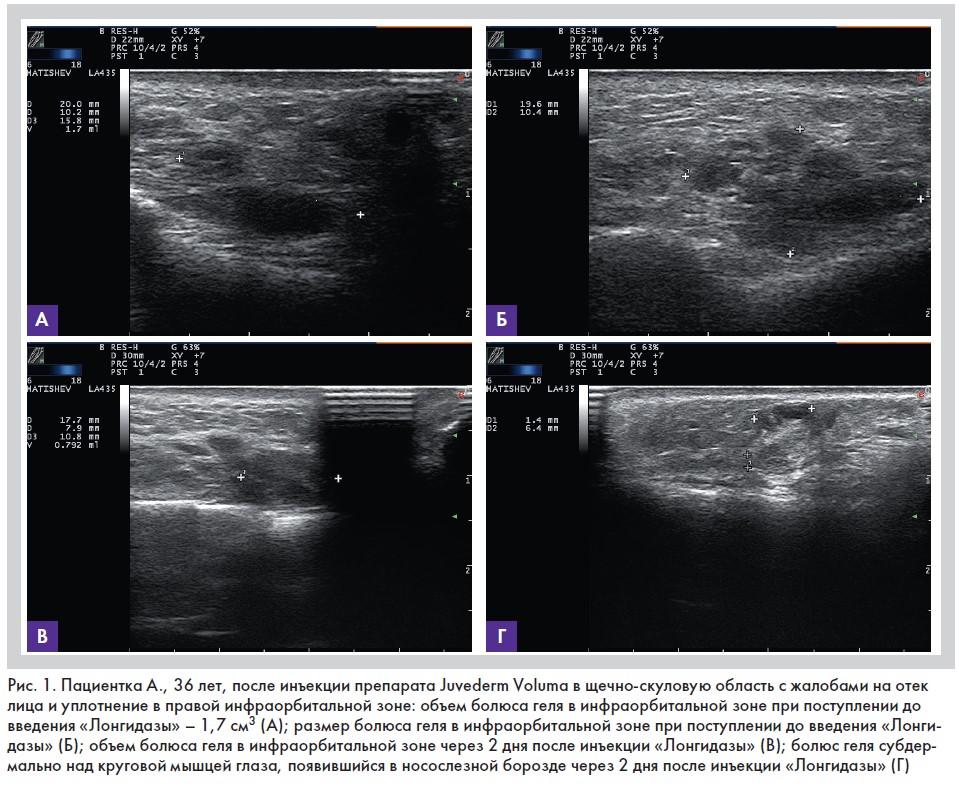
У двух пациентов после многократных (8- и 11-кратных) инъекций препаратов гиалуронидазы в область зоны введения геля Restylane Perlane (носослезные борозды и область скуловой кости), обследованных после последнего введения гиалуронидазы на 7-е и 14-е сутки, находили локусы геля в зонах введения без признаков биодеградации. Причем в одном из случаев, описанном в клиническом примере ниже, делали УЗИ на 7-й день после введения препарата гиалуронидазы и на 49-й день, при этом размеры болюса филлера были без динамики. Препарат Juvederm Voluma у пациента А. с клинической картиной персистирующих отеков, введенный в щечно-скуловую зону в объеме 0,4 мл с каждой стороны, увеличился с правой стороны, по данным УЗИ, в три раза от исходного объема, и его фактический объем составил 1,7 см3 (рис. 1А). При этом препарат мигрировал с обеих сторон из зоны инъекции в область скуловой кости, в
инфраорбитальную область, лоцировался в fossa canina и контактировал с веточками подглазничного (инфраорбитального) сосудисто-нервного пучка, хорошо пальпировался как уплотнение тканей (рис. 1Б). После введения препарата
«Лонгидаза» на вторые сутки локус геля с правой стороны уменьшился в два раза, но при этом все равно оставался в полтора раза больше от исходного введенного объема – 0,7 см3 (рис. 1В). С противоположной стороны размеры
локуса до введения «Лонгидазы» и на вторые сутки после введения были без динамики, по 0,4 см3. Интересен тот факт, что при контрольном исследовании после введения «Лонгидазы» гель обнаружили в носослезной борозде подкожно (рис. 1Г). При первичном осмотре на УЗИ геля в этой зоне не было, и изначально в зону носослезных борозд гель не вводился. Создается впечатление, что в зоне отека тканей лицевого скелета гель мигрировал предположительно по градиенту давления. Индекс резистентности (ИР) при доплеровском исследовании (ДИ) лицевой артерии при поступлении и контрольном осмотре на вторые сутки после введения «Лонгидазы» с обеих сторон был снижен до 0,50. Пациенту назначили фонофорез с однопроцентной гидрокортизоновой мазью. В динамике на десятые сутки после инъекции «Лонгидазы» и шести процедур фонофореза с однопроцентной гидрокортизоновой мазью у пациента наступило значительное
улучшение клинической картины, уменьшился отек лица, пальпаторно ткани лица стали мягкие, фактический объем болюса в правой инфраорбитальной области составил 0,33 см3, ИР вырос с 0,50 до 0,61 (рис. 2).
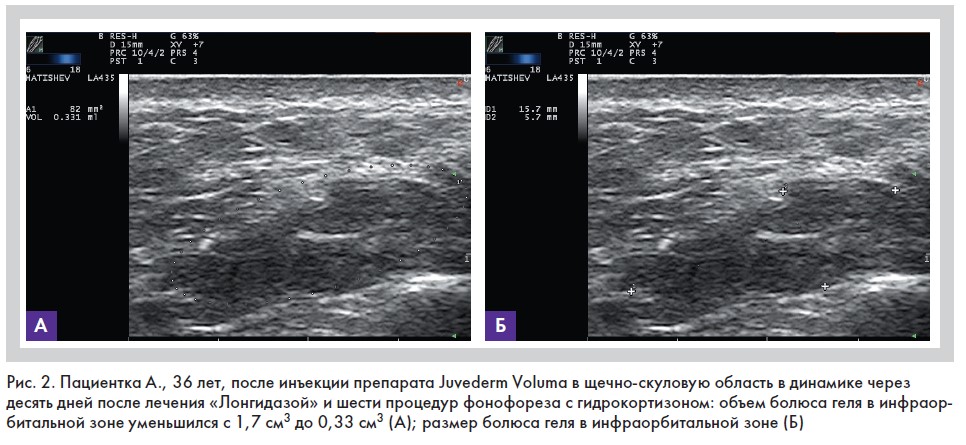
У пациента с жалобами на гиперкоррекцию спустя девять месяцев после инъекции препарата Juvederm Ultra 3 в губы на границе перехода красной каймы в слизистую была выявлена УЗИ картина фиброза в виде гиперэхогенного тяжа на красной кайме нижней губы, который ошибочно трактовался пациентом как болюс филлера.
У пациента с жалобами на гиперкоррекцию в области лба после инъекции филлера трехгодичной давности в Китае, предположительно биополимерной природы, по всему лицу лоцировались анэхогенные болюсы неправильной формы в гиподерме, а в области лба – субдермально. У другой пациентки с жалобами на асимметрию губ после хирургического удаления гранулемы, развившейся после введения геля неустановленной природы, его неудаленные остатки визуализировались по типу «яйца моли в паутине».
У пациента с синдромом Мелькерссона-Розенталя гель Restylane Perlane в области скуловой кости визуализировался в виде четких анэхогенных локусов. У него же в губах визуализировался Restylane с признаками неполной биодеградации в виде анэхогенных и гипоэхогенных локусов спустя 14 месяцев после инъекции. Синдром развился за два месяца до обследования и, по нашему мнению, не связан с наличием филлера. Нам показался интересным тот факт, что спустя 14 месяцев после инъекции филлер полностью не биодеградировал.
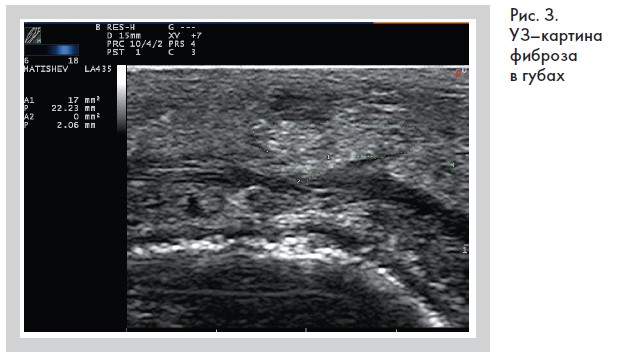
У остальных 16 пациентов с жалобами на отечность, асимметрию и гиперкоррекцию сонографическая картина геля на основе гиалуроновой кислоты сочеталась с ультразвуковыми признаками отека жировой ткани по типу септального панникулита в четырех случаях, фиброзом – в 11. Очаги фиброза размером от четырех миллиметров и более в диаметре хорошо пальпировались в губах (у трех человек) (рис. 3), воспринимаясь пациентами как «нерассосавшийся гель», а также в мягких тканях лица (у двух человек).
После окончания первого этапа лечения у пациентов с гелями на основе гиалуроновой кислоты (80%) наблюдали положительную динамику, а именно уменьшение размеров болюсов и изменение их структуры из четко лоцируемых
гипоэхогенных и анэхогенных образований до лечения в неоднородные структуры, замещающиеся эхопозитивной тканью, предположительно фиброзной. На степень биодеградации и уменьшение размера геля, по нашим наблюдениям, влияла глубина залегания и размер исходного болюса. Чем глубже находился болюс и больше был его размер, тем хуже он поддавался коррекции. В области fossa canina и подбородка гель медленней всего поддавался терапии, уменьшаясь не более чем на 25% от исходного размера, в то время как гель с более поверхностным залеганием уменьшался после первого этапа лечения на 40–60% и приобретал при ультразвуковом исследовании вид неоднородных фрагментированных структур повышенной эхогенности, что косвенно свидетельствовало о замещении болюса филлера соединительной тканью (фиброзирование).
Специалисты Клинического центра челюстно-лицевой, реконструктивно-восстановительной и пластической хирургии Клиники МГМСУ им. А.И. Евдокимова в своей работе описали различные варианты исхода введенного филлера по данным эхографического исследования в динамике. Наши наблюдения совпадают с данными исследователей. Исход после контурной пластики гелями на основе гиалуроновой кислоты – это фиброз с различной степенью выраженности [5].
Интересен тот факт, что из 10 пациентов (50% от общего числа обследованных), предъявлявших жалобы на гиперкоррекцию носослезных борозд, только у пяти (25%) гель в области носослезной борозды определяли как над
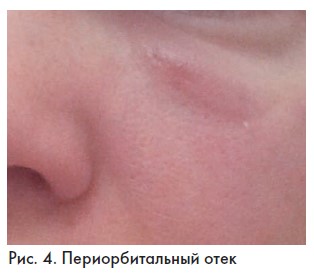
круговой мышцей глаза, так и под ней, при этом присутствовала клиника отека периорбитальной зоны. У оставшихся пяти человек (25%) гель находился под круговой мышцей глаза, и также присутствовала клиническая картина отека
указанной области, которая воспринималась как гиперкоррекция (рис. 4).
У этих же 10 пациентов (50% обследованных) в 30% случаев (шесть человек) гель лоцировался в инфраорбитальной области (fossa canina) в глубоких слоях. Еще у пяти пациентов (25%) в области носослезной борозды гель визуализировался вдоль угловой артерии и дорсальной артерии носа. При этом у пяти обследованных пациентов (25%) гель находился не просто вдоль сосуда, а контактировал с ним на разных участках: в 2 случаях (10%) с лицевой артерией
в проекции носослезной борозды и еще в 2 случаях (10%) – на уровне выхода подглазничных артерии и нерва. У этих пятерых пациентов (25%) наблюдалось снижение индекса резистентности (ИР) при доплеровском исследовании лицевой артерии и ее ветвей, что коррелировало с клиникой длительно сохраняющихся (более трех недель) отеков. Индекс резистентности был снижен во всех точках сосуда, с которым контактировал гель. При этом у пациентов с расположением геля вдоль сосуда, но не прилегавшего к нему снижения ИР не отмечалось. Предположительно механизм снижения ИР может быть связан с дисбалансом релаксирующих и констриктирующих факторов, один из которых – оксид азота. Так, например, в работах по изучению патогенеза развития постгеморрагического церебрального вазоспазма установлено, что в острый период наблюдается высокая функциональная нитроксидергическая вазорелаксация. Со второй недели геморрагического периода отмечаются различия по клиническому течению заболевания и динамике показателей состояния нитроксидергической вазорелаксации: при отсутствии ишемических осложнений уровень нитрита находился
в пределах нормы, а апоплектиформный вазоспазм, напротив, протекал на фоне значительного снижения уровня нитрита относительно нормы [6].
В другом исследовании по изучению патогенеза развития инфекционно-токсического шока было установлено значительное повышение уровня нитрита как метаболита оксида азота у больных с клиникой инфекционно-токсического шока, чего не наблюдалось в группе тяжелых больных без клиники шока [7]. Описанный в работах Карповой Е.И., Мингазовой Л.Р., Орловой О.Р. компрессионно-ишемический синдром, нейропатические расстройства в области лица после контурной
инъекционной пластики могут приводить к такому дисбалансу релаксирующих и констриктирующих факторов [8, 9]. Однако данный вопрос требует дополнительных исследований. В пользу того, что немеханическое сдавление гелем может поддерживать клиническую картину персистирующих отеков, свидетельствует другое исследование. Экспериментальная работа на мышах показала, что при максимальном уровне давления и растяжения мягких тканей филлерами, введенными в область проекции сосуда, значительных изменений со стороны функционирования сосудистого русла не выявлено [10]. Наши исследования косвенно подтверждают клинические проявления инструментальным методом.
Определение индекса резистентности может быть использовано для дифференциальной диагностики компрессионно-ишемического синдрома в области лица.
После первого этапа лечения пациентам с размерами локусов геля более 3 мм в диаметре (25% обследованных) понадобился второй этап лечения – введение препарата «Лонгидаза» под контролем УЗИ. Через две недели осуществлен повторный УЗ-контроль. В зоне введения наблюдались признаки редукции, биодеградации и фрагментации геля на отдельные изоэхогенные участки размерами менее 1–2 мм.
Клинические примеры
Пример 1. Пациентка Б., 25 лет, обратилась с жалобами на гиперкоррекцию и асимметрию после введения гелей на основе гиалуроновой кислоты в область носослезных борозд и скул слева. Пациентке неоднократно вводили гели
различных производителей в указанные зоны. После предпоследней коррекции в область носослезных борозд был введен гель Restylane Perlane, который пациент пытался убрать в связи с возникшей асимметрией с помощью неоднократных инъекций препаратов на основе фермента гиалуронидазы. Каждый раз после инъекции возникал локальный отек в зоне введения препарата, сохраняющийся от нескольких дней до нескольких недель. После третьей попытки убрать филлер в области носослезных борозд препаратами гиалуронидазы пациентке был введен в эту зону гель Juvederm Volbella с целью коррекции сохраняющейся асимметрии. Так как асимметрия не была скорректирована, попытки разрушить гель препаратами гиалуронидазы были продолжены (всего их было восемь). Нам так и не удалось выяснить названия препаратов гиалуронидазы, вводившихся пациентке, а также дозу однократного введения. Пациентка пришла на первичный
прием с клиникой ярко выраженных отеков в области глаз. При пальпации в области левой скулы определялось уплотнение. Пациентке провели диагностическое ультразвуковое исследование мягких тканей периорбитальных
и скуловых областей на седьмой день после последней инъекции гиалуронидазы. Параорбитально слева нечетко прослеживался гипоэхогенный локус филлера в фазе начальной редукции толщиной до 1,3 мм и длиной до 2,1 мм с отеком окружающей клетчатки в виде муфты до 6 мм в диаметре. В зоне пальпируемого образования над скуловой костью слева в подкожно-жировой клетчатке (ПЖК) лоцировался очаговый отек с анэхогенными включениями неправильной формы общим размером до 9,2 х 4,1 х 6,1 мм.
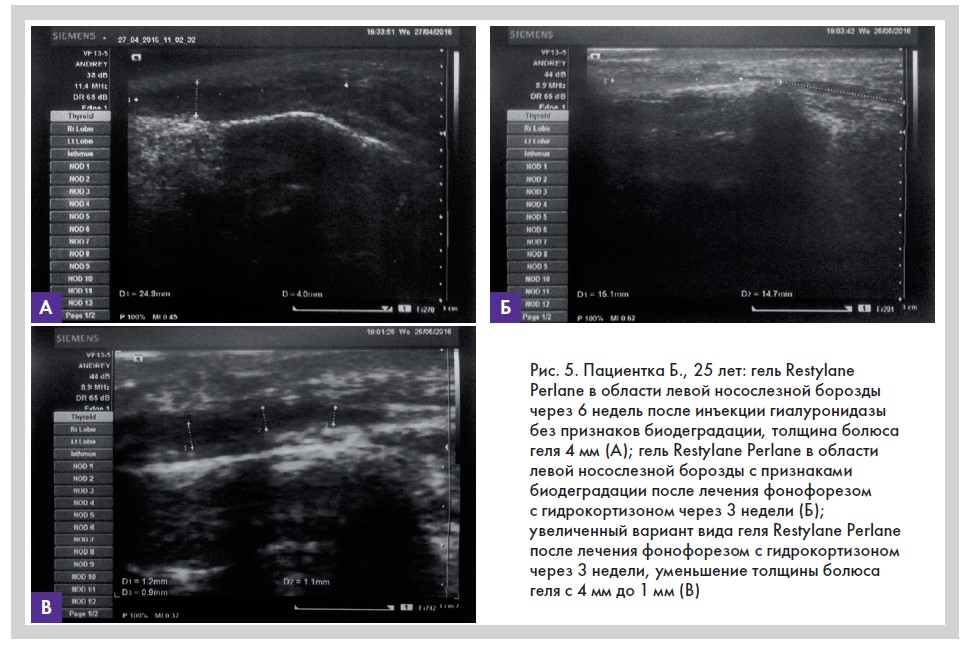
В связи с недавним введением препарата гиалуронидазы в зоны гиперкоррекции пациентке предложили подождать 3–4 недели с последующим ультразвуковым контролем для оценки динамики. Повторное УЗИ через шесть недель показало положительную динамику в отношении интенсивности отека и отсутствие динамики в отношении структуры геля. В левой носослезной борозде четко визуализировался гипоэхогенный болюс геля длиной 24,9 мм, толщиной 4,0 мм (рис. 5А). В области левой скулы лоцировались два гипоэхогенных болюса размером 6,3 х 3,2 мм и 5,1 х 2,1 мм. УЗ-контроль наглядно продемонстрировал отсутствие желаемого клинического эффекта от бесконтрольного лечения гиперкоррекции
препаратами гиалуронидазы без учета топики зоны введения, да еще и на фоне отсутствия каких-либо четких рекомендаций по дозировкам. Пациентке было назначено лечение: фонофорез с однопроцентной гидрокортизоновой
мазью по четыре минуты однократно, ежедневно курсом 10 сеансов. На контрольном УЗИ через три недели после окончания курса лечения выявлена положительная динамика. Гель в области левой носослезной борозды из цельной полоски до лечения был фрагментирован на несколько участков с максимальной толщиной 1,2 мм, 0,9 мм и 1,1 мм (до лечения толщина составляла 4 мм) (рис. 5Б, 5В). Размер болюсов в области левой скулы составил 3,3 х 1,6 мм и 2,9 х 1,4 мм соответственно против 6,3 х 3,2 мм и 5,1 х 2,1 мм до лечения, причем с явными признаками биодеградации, проявляющейся при ультразвуковом исследовании в виде неоднородной структуры болюсов повышенной эхогенности (предположительно фиброзная ткань). Общий размер болюсов геля после первого этапа лечения сократился в 2–3 раза. На втором этапе лечения непосредственно в болюс геля в области левой скулы размером 3,3 х 1,6 мм под УЗ-контролем, минуя прилежащие сосуды и нервы, ввели 75 МЕ препарата «Лонгидаза». Через две недели повторно проведен УЗ-контроль. В зоне введения лоцировались признаки редукции, биодеградации и фрагментации геля на отдельные
изоэхогенные участки размерами менее одного миллиметра. Пальпаторно ткани однородны.
Пример 2. Пациентка В., 25 лет, с жалобами на гиперкоррекцию и асимметрию после введения гелей на основе гиалуроновой кислоты в область губ. Пациентку беспокоила гиперкоррекция правой латеральной части верхней губы и асимметрия относительно левой, а также эстетическая неудовлетворенность формой губ. Пациентка изъявляла желание избавиться от асимметрии и вернуть прежнюю форму губ. До обращения за помощью она предпринимала попытку убрать гель введением одномоментно двух флаконов препарата «Лонгидаза», после чего, с ее слов, развилась клиника отека Квинке с отеком всего лица и шеи. После купирования отека сохранялась асимметрия губ и пальпировалось уплотнение в правой латеральной части верхней губы.
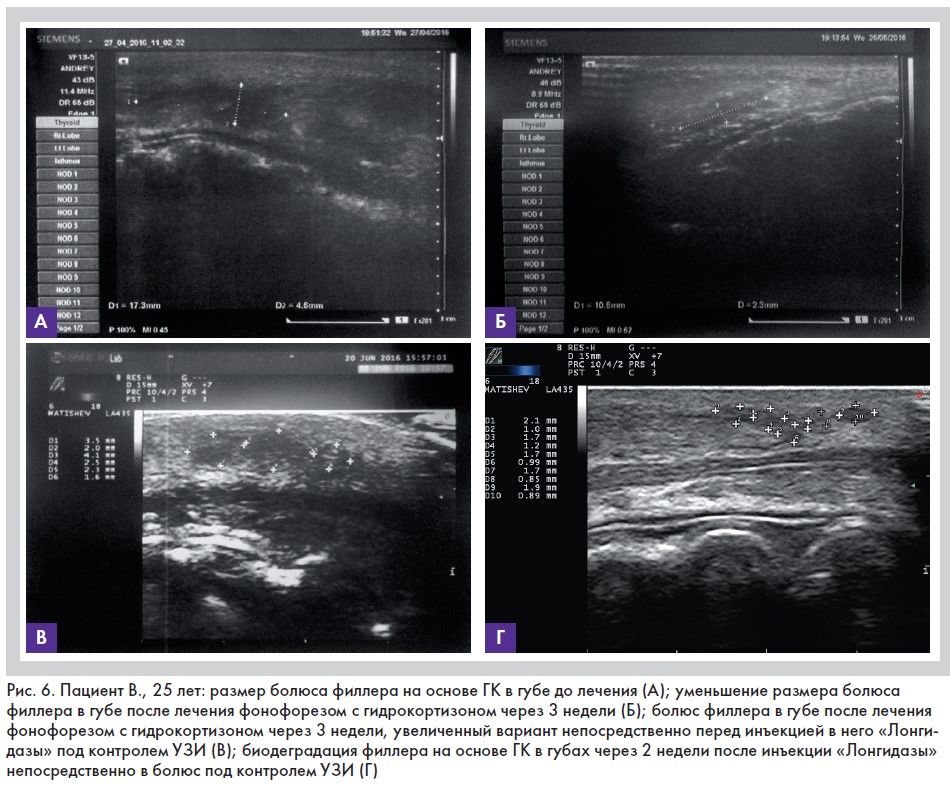
При осмотре пациентки губы асимметричны, пальпаторно в области правой латеральной части верхней губы отмечается уплотнение. При первичном обращении проведено диагностическое ультразвуковое исследование губ. Обнаружен гель, неравномерно располагающийся в тканях верхней губы в виде отдельных болюсов размером от 2,9 мм до 3,9 мм. Самый большой из них – в области правой латеральной части верхней губы длиной 17,3 мм, толщиной 4,6 мм (рис. 6А). Структура ткани губы неоднородна, с признаками выраженного фиброза (рис. 3).
Пациентке назначено лечение: фонофорез с однопроцентной гидрокортизоновой мазью по четыре минуты однократно, ежедневно курсом 10 сеансов. УЗ-контроль через три недели после окончания первого этапа лечения показал положительную динамику. Уменьшился размер болюсов и изменилась их структура из четко визуализирующихся гипоэхогенных, анэхогенных образований до лечения в неоднородные структуры, замещающиеся эхопозитивной тканью, предположительно фиброзной. Самый крупный болюс – в правой латеральной части верхней губы уменьшился с 17,3 х 4,6 мм до 10,6 х 2,3 мм (рис. 6Б). Однако в этой зоне сохранялась легкая асимметрия и пальпировалось уплотнение. Пациентке провели второй этап коррекции, а именно ввели препарат «Лонгидаза» 75 МЕ под УЗ-контролем непосредственно в область локации геля (рис. 6В). Через две недели в зоне введения УЗ-контроль показал признаки редукции, биодеградации и фрагментации геля на отдельные изоэхогенные участки размерами менее 1–2 мм, неоднородные по структуре (рис. 6Г). Визуально губы выглядят симметрично, при пальпации – структура ткани губы однородна.
И в заключение
1. При контакте геля с сосудом наблюдается снижение индекса резистентности при ДИ.
2. Бесконтрольное введение препаратов гиалуронидазы в зону гиперкоррекции гелем на основе ГК не вызывает полной биодеградации филлера.
3. Фонофорез с однопроцентной гидрокортизоновой мазью является эффективным альтернативным методом лечения нежелательных явлений контурной пластики филлерами на основе ГК.
4. Филлеры на основе ГК в глубоких слоях тканей лица хуже и медленней поддаются процессу лечения препаратами гиалуронидазы и фонофорезу с однопроцентной гидрокортизоновой мазью.
5. Максимального эффекта от терапии нежелательных явлений контурной пластики гелями на основе ГК мы добиваемся при сочетании ультразвукового фонофореза с однопроцентной гидрокортизоновой мазью с последующим введением препаратов гиалуронидазы под контролем УЗ.
6. Исход после контурной пластики гелями на основе ГК – фиброз различной степени выраженности.
ЛИТЕРАТУРА
[1] Инъекционные методы в косметологии / под ред. Б. Ашера; пер. с англ.; под ред. Н.П. Михайловой. – М.: МЕДпресс-информ, 2016. – 584 с.
[2] Илешина Т.В. Осложнения инъекционных методов коррекции в эстетической медицине // Метаморфозы. – 2013. – № 2. – С. 48–52.
[3] Озерская О.С. Рубцы кожи и их дерматокосметологическая коррекция. – СПб.: Искусство России, 2007. – 224 с.
[4] Бутов С.Н., Ахтямов Ю.С. Практическая дерматокосметология. – М.: Медицина, 2003. – 397 с.
[5] Роль ультразвукового исследования высокого разрешения в диагностике осложнений контурной пластики лица / Е.Г. Привалова, Е.И. Губанова, А.Ю. Васильев, Д.В. Давыдов // Метаморфозы. – 2017. – № 18.
[6] Карпюк В.Б. Состояние нитроксидергической вазорелаксации при субарахноидальном кровоизлиянии (клинико-патогенетические аспекты церебрального вазоспазма): автореф. дис. … канд. мед. наук. – М., 2001. – 29 с.
[7] Бондаренко И.Н. Клинико-патогенетическое и прогностическое значение оксида азота при лептоспирозе: дис. … канд. мед. наук. – Краснодар, 2008. – 129 с.
[8] Карпова Е.И. Компрессионно-ишемический синдром в практике косметолога // Метаморфозы. – 2014. – № 5. – С. 54–58.
[9] Осложнения в виде нейропатических расстройств в области лица после контурной инъекционной пластики / Л.Р. Мингазова, Е.И. Карпова, О.Р. Орлова, К.В. Котенко, Л.С. Круглова // Российский журнал кожных и венерических болезней. – 2014. – № 3. – С. 52–55.
[10] Кореневская А.Я., Ширшакова М.А. Куда попадают филлеры? Визуальная диагностика тканевых наполнителей // Метаморфозы. – 2017. – № 17. – С. 16–22.
