Бычкова Наталья Юрьевна, к.м.н., доцент кафедры эстетической медицины РУДН, член профильной комиссии по дерматовенерологии и косметологии МЗ РФ, главный внештатный специалист по косметологии МЗ Удмуртии, президент Ассоциации «Секция эстетической медицины», председатель экспертного совета по лечению осложнений в косметологии, Москва
Наумова Наталья Георгиевна, к.м.н., доцент, заведующая кафедрой биохимии ФГБОУ ВО ИГМА Минздрава России, Ижевск
Старение лица представляет собой многофакторный процесс, при котором происходят выраженные изменения различных структур. Эпидермальная дисфункция, снижение функциональной активности клеток и дезорганизация внеклеточного матрикса дермы, атрофия и дислокация жировых компартментов в сочетании с дисбалансом мышц и потерей объема подлежащих костных структур приводят к формированию морщин, нарушениям конфигурации и «дряблому виду» кожи лица [7]. Наблюдаемые изменения кожного рельефа являются отражением тех сложных структурных деформаций, которые происходят в многослойном, морфологически неоднородном органе, содержащем ткани с сильно отличающимися механическими и функциональными характеристиками. Хроническое фотоповреждение в значительной степени усугубляет эти процессы: образуются активные формы кислорода (АФК), активируются митоген-активируемые протеинкиназы (MAPKs) и индуцирующие факторы транскрипции. Это увеличивает активацию матриксных металлопротеиназ (ММП) и ингибирование передачи сигналов трансформирующего фактора роста-β (TGF-β), что приводит к фрагментации и снижению синтеза коллагена, ухудшая механическое взаимодействие между дермальными структурами. Стареющие фибробласты продуцируют большее количество АФК, что еще больше увеличивает экспрессию ММП и ингибирует сигнализацию TGF-β, создавая положительную обратную связь, которая ускоряет старение кожи [10, 16, 17].
Клиническим отражением этих процессов является усиление дермального рисунка, гиперкератоз, тусклость, дисхромия, появление морщин, пастозность, нарушения конфигурации. Происходит провисание щек, образование мешков под глазами, нависание век, углубление складок и борозд, деформация овала лица. С возрастом проявления старения усугубляются, наблюдается увеличение складчатости и дальнейшее снижение тургора кожи,
птоз мягких тканей с аккумуляцией подкожного жира и без него, деформация формы анатомических структур лица, появление или усугубление складок и борозд. Сосудистый компонент выражается отечностью, расширением
капилляров (телеангиэктазии) и появлением «синевы» в области медиальных углов глаз, может наблюдаться одутловатость в области век или всего лица.
Способы коррекции возрастных изменений
На сегодняшний день в арсенале специалистов имеется большое количество инъекционных и аппаратных методов, позволяющих эффективно воздействовать на клинические проявления, наблюдаемые при старении. Исследователями предлагаются различные способы коррекции возрастассоциированных изменений мягких тканей в зависимости от клинических, возрастных и этнических особенностей [5, 11, 13, 15, 19, 20, 21]. Стратегии терапии и рекомендации по комбинациям применяемых методов основаны на результатах научных исследований и клиническом опыте экспертов, анализе индивидуальных особенностей пациента, имеющейся коморбидной
патологии, косметологического анамнеза. Для повышения эффективности эстетической коррекции важны знания патофизиологии старения, понимание этапности процессов коррекции, включающих мышечный контроль, восстановление объема и реконтурирование, а также компенсацию дисфункциональных метаболических дермальных нарушений [1, 4, 19]. В комплексных протоколах терапии широко используются инъекционные методы.
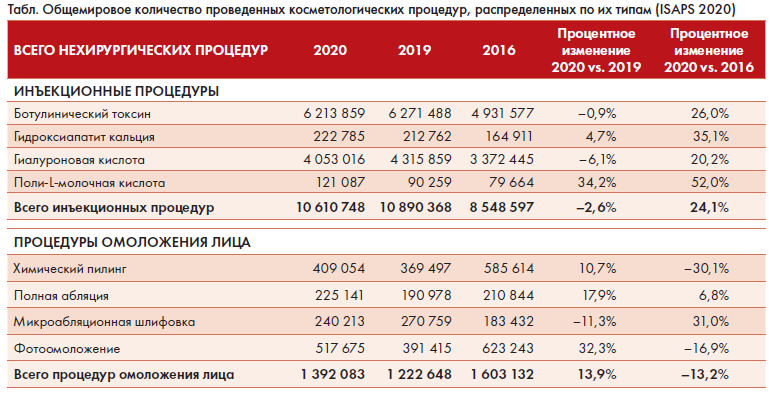
По результатам глобального опроса, ежегодно проводимого Международным обществом эстетической пластической хирургии (ISAPS), число нехирургических процедур, выполненных в 2020 г., составило 14 400 347 случаев,
из них большую часть (10 610 748 случаев – 73,7%) занимали инъекционные методы (табл.), при этом за период с 2016 по 2020 г. наиболее существенное увеличение продемонстрировали методы инъекционной коллагеностимуляции: число процедур с применением гидроксиапатита кальция увеличилось на 35,1%, а с применением препаратов полимолочной кислоты – на 52% [9]. Таким образом, одной из наиболее перспективных и развивающихся направлений инъекционной косметологии является имплантация препаратов полимолочной кислоты (PLA).
Инъекционные препараты полимолочной кислоты для коррекции возрастных изменений
В нашем организме молочная кислота (лактид, 2-гидроксипропионовая кислота, LA) образуется постоянно и участвует во многих обменных процессах. Впервые она была выделена из ферментированного молока в 1970 г. Карлом Шееле. В ее молекуле имеется асимметричный атом углерода, который обусловливает существование двух форм (энантиомеров): L-молочная кислота и D-молочная кислота. Молочная кислота, полученная из мышц животных, представляет собой правовращающую молочную кислоту, тогда как молочная кислота, полученная путем ферментации, представляет собой левовращающую молочную кислоту [12].
Полимолочная кислота (полилактид, PLA)- синтезируемый биоразлагаемый биосовместимый полимер, мономером которого является молочная кислота, получаемая в результате ферментации кукурузного крахмала, свекольного сахара и других природных источников. Сегодня PLA одобрена FDA и европейскими регулирующими органами для использования в системах доставки продуктов питания и лекарств [8, 12].
Важной особенностью PLA является безопасность и прогнозируемая биодеградация в биологических тканях, поэтому первоначально она применялась в медицине в виде хирургических нитей, фиксационных стержней и костных штифтов, впоследствии области ее применения значительно расширились. В косметологии инъекционные имплантаты на основе L-формы полилактида (PLLA) применяются около 20 лет, и в настоящее время накоплен
большой опыт эффективного и безопасного их использования [1, 2, 8, 15]. Инъекционная поли-D,L-молочная кислота (PDLLA) — новый наполнитель, получивший распространение в последние годы [6].
По сравнению с традиционными дермальными наполнителями (филлерами) имплантаты на основе полимолочной кислоты обладают эффектом биологической стимуляции, усиливая синтез эндогенного коллагена и активизируя работу дермальных фибробластов после инъекции. Стимулирующее влияние PLA достаточно выражено и сохраняется в течение двух и более лет [8].
Молочная кислота является энергетическим субстратом и оказывает влияние на метаболическую функцию клеток [18]. Из-за своего небольшого размера она может проникать через липидную мембрану клеток посредством
челночной системы белков-транспортеров монокарбоксилатов, или «лактатных челноков» [3]. Последние исследования показывают, что лактат служит ключевым компонентом обменных процессов, он образуется и непрерывно используется в различных клетках. Концепции «клетка-клетка» и «внутриклеточный лактатный челнок» описывают роль лактата в доставке окислительных и глюконеогенных субстратов, а также в передаче клеточных сигналов. Наличие лактатных челноков приводит к осознанию того, что гликолитический и окислительный пути следует рассматривать как связанные, а не альтернативные процессы [3]. Также было показано, что LA обладает антиоксидантными свойствами, которые могут служить для защиты клеток от повреждения, вызванного свободными радикалами [18]. Оказывая влияние на регуляцию окислительно-восстановительного потенциала клеток,
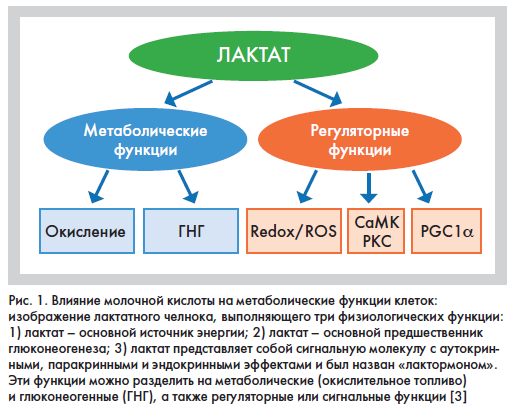
аллостерического связывания и перепрограммирования хроматина путем лактилирования остатков лизина на гистонах, лактат играет большую роль в распределении энергии в клетках, выполняя метаболические (окислительное топливо) и регуляторные или сигнальные функции (рис. 1). Считается (Джордж Брукс, 2020), что изменение концентрации лактата в ткани оказывает быстрое и значительное воздействие на окислительно-восстановительный потенциал клеток и другие системы контроля. Физиологический диапазон тканевого лактата составляет 0,5–20 мМ, и эти величины могут существенно меняться во время физической нагрузки и стрессовых реакций, превышая другие метаболические сигналы по величине и продолжительности. Особенности эпигенетической регуляции генов с помощью лактилирования гистонов только начинают изучать, но в будущем будет возможно оценить краткосрочные и долгосрочные эффекты влияния этого механизма на митохондриальный биогенез и экспрессию других метаболических белков после физических упражнений и режимов тренировок, а также при различных острых и хронических заболеваниях и состояниях, таких как старение, диабет, сепсис и заживление ран [3].
Характеристика инъекционных препаратов полимолочной кислоты
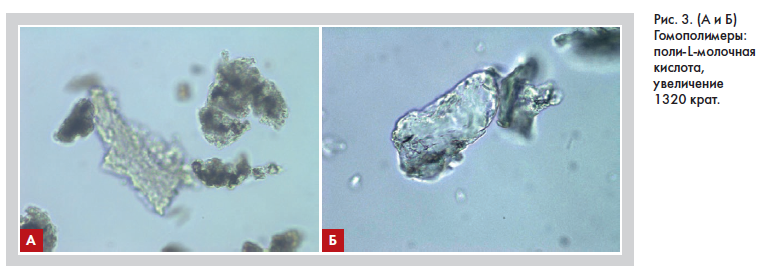
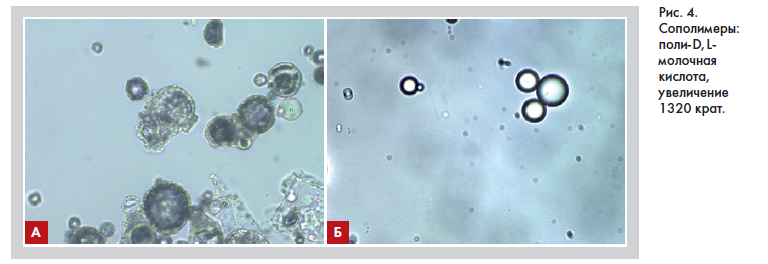
В России в настоящее время зарегистрированы следующие интрадермальные имплантаты (филлеры) полимолочной кислоты (рис. 3, 4):
I. гомополимеры (поли-L-молочная кислота, PLLA) – имплантат для подкожного введения SCULPTRA™ (Кью-Мед АБ, Швеция, РУ № ФСЗ 2009/05553 от 03.04.2017), имплантатдля инъекционной коррекции морщин и восполнения объема GANA V/GANA Х (GANA R&D Co Ltd, Корея, РУ № РЗН 2021/13973 от 08.04.2021);
II. сополимеры (поли-D,L-молочная кислота, PDLLA) – дермальный филлер для инъекционной коррекции морщин и восполнения объема AestheFill® V200, материал инъекционный для мужской и женской интимной пластики PowerFill («РЭДЖН Биотэк, инк.», Корея, РУ № РЗН 2018/7416 от 04.03.2019; РУ № РЗН 2018/7434 от 04.03.2019), дермальный филлер для коррекции морщин и восполнения объема Repart® PLA (ООО «ИНГАЛ», Россия, РУ № РЗН 2021/15926 от 06.12.2021).
Все инъекционные интрадермальные имплантаты PLA представляют собой наполнитель, содержащий кристаллы или микросферы полилактида и карбоксиметилцеллюлозу (КМЦ), которая используется для повышения вязкости системы и предотвращения агрегации частиц PLA, что может вызвать неравномерное распределение в тканях, привести к гиперстимуляции и образованию гранулем. Маннитол, входящий в состав большинства препаратов, представляет собой защитный агент и обладает антиоксидантной активностью, поглощая свободные радикалы в организме, ингибируя быструю деградацию наполнителя и снижая риск отека после инъекции. Перед инъекцией необходимо восстановить инъекционный препарат PLA стерильной водой для инъекций (SWFI) для образования гомогенной суспензии. Был проведен ряд исследований, демонстрирующих, что применение других растворителей повышает риск развития осложнений [6, 14].
Repart® PLA – новый отечественный препарат полимолочной кислоты
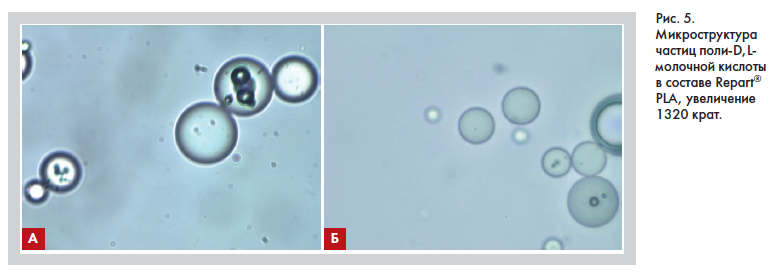
Большой интерес на сегодняшний день представляет отечественный препарат полимолочной кислоты Repart® PLA (рис. 5), который производится в научно-производственном комплексе ИНГАЛ (Ingal). Эта современная производственная площадка организована в соответствии с международными стандартами осуществления фармацевтической деятельности ISO и EU GMP. Научно-производственный комплекс оснащен самым современным роботизированным оборудованием, осуществляется тщательный контроль производственного процесса на каждом этапе. В качестве сырья при производстве Repart® PLA используется высокоочищенная субстанция мирового лидера по производству биоразлагаемых полимеров – немецкого фармацевтического концерна EVONIK.
В состав комплекса ИНГАЛ входит научно-исследовательская лаборатория (R&D центр), которая занимается исследованием неньютоновских псевдопластичных жидкостей и биоразлагаемых полимеров. Разрабатываются,
патентуются и внедряются в производственный процесс собственные технологии производства. Большой опыт выпуска лиофилизированных лекарственных средств позволил специалистам компании ИНГАЛ разработать собственную уникальную технологию двойной лиофилизации для производства препарата на основе полиD,L-молочной кислоты III поколения Repart® PLA, позволяющую получить препарат со стандартизированным размером микрочастиц, имеющих правильную сферическую форму с гладкой поверхностью. В состав изделия входит оптимальная концентрация поли-D,L-молочной кислоты – 154 мг, натрия карбоксиметилцеллюлоза – 46 мг и маннитол – 167,2 мг. Технологический процесс включает несколько этапов: эмульгирование субстанции PLA, созревание микросфер с заданными гранулометрическими параметрами, двойная лиофилизация с получением сухой пористой массы и стерилизация радиоактивным методом.
Таким образом, благодаря разработке и внедрению новой технологии двойной лиофилизации удалось создать эффективный продукт III поколения Repart® PLA со следующими важными характеристиками.
Для специалиста:
– время приготовления рабочей суспензии сокращено до трех минут;
– идеальная сферичная форма микрочастиц PLA обусловливает равномерное распределение в тканях;
– иглы и канюли не закупориваются в процессе работы.
Для пациента:
– высокая комфортность процедуры, нет отеков и болезненности;
– отсутствие необходимости в проведении массажа после имплантации;
– результат наблюдается в течение первого месяца после имплантации и сохраняется до 2 лет.
Показания к применению препарата Repart® PLA
Показаниями к применению Repart® PLA являются возрастные изменения кожи лица, шеи, декольте: мимические и статические морщины различной степени выраженности, улучшение рельефа кожи, увеличение и/или восстановление объема мягких тканей лица (щечно-скуловой и височной областей, нижней трети лица), коррекция возрастных изменений и создание дополнительного объема кожи и подкожной клетчатки кистей рук. Демонстрационные клинические примеры приведены на рис. 6 и 7.
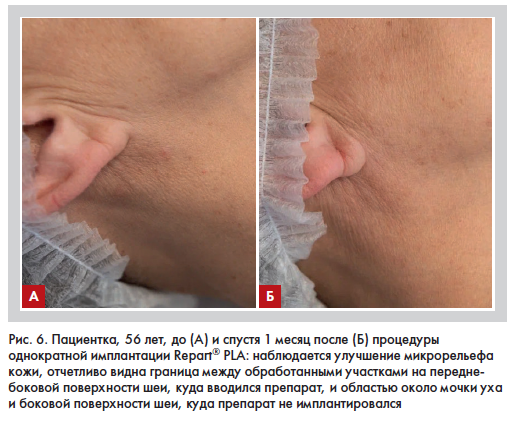
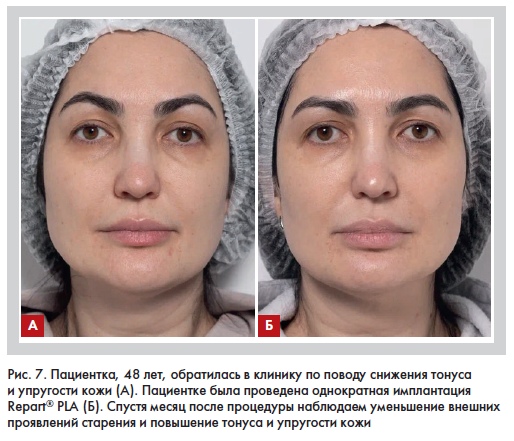
После проведения процедуры наблюдается восполнение утраченных объемов мягких тканей, заполнение морщин, складок и областей депрессии, выравнивание микрорельефа кожи, повышение ее тургора и эластичности.
Курс терапии составляет от 1 до 3 процедур и зависит от выраженности возраст-ассоциированных изменений мягких тканей. Наш опыт показывает, что даже после однократного применения препарата Repart® PLA пациенты
отмечают значительное повышение упругости кожи, разглаживание мелких морщин, уменьшение глубины складок и заломов, снижение выраженности гравитационного птоза (рис. 7).
И в заключение
1. Таким образом, возрастные изменения дермы сопровождаются нарушением структуры и функции стромы кожи и ее механических свойств (фибриллярного каркаса и внеклеточного матрикса).
2. Использование препаратов на основе полимолочной кислоты является патогенетически обоснованным способом терапии, позволяющим компенсировать энергетический дефицит и нормализовать процессы синтеза всех компонентов дермального матрикса.
3. После применения препарата Repart® PLA пациенты отмечают значительное повышение упругости кожи, разглаживание мелких морщин, уменьшение глубины складок и заломов, снижение выраженности гравитационного
птоза.
Литература
[1] Akinbiyi T., Othman S., Familusi O., Calvert C., Card E.B., Percec I. Better Results in Facial Rejuvenation with Fillers. Plast Reconstr Surg Glob Open. 2020 Oct 15; 8(10): e2763. doi:10.1097/GOX.0000000000002763. PMID: 33173655; PMCID:PMC7647625.
[2] Alessio R., Rzany B., Eve L., Grangier Y., Herranz P., Olivier-Masveyraud F., Vleggaar D. European expert recommendations on the use of injectable poly-L-lactic acid for facial rejuvenation. J Drugs Dermatol. 2014 Sep; 13(9): 1057–1066. PMID: 25226006.
[3] Brooks G.A. Lactate as a fulcrum of metabolism. Redox Biol. 2020 Aug; 35:101454. doi: 10.1016/j.redox.2020.101454. Epub 2020 Feb 9. PMID: 32113910; PMCID: PMC7284908.
[4] Carruthers J., Burgess C., Day D., Fabi S.G., Goldie K., Kerscher M., Nikolis A., Pavicic T., Rho N.K., Rzany B., Sattler G., Sattler S., Seo K., Werschler W.P., Carruthers A. Consensus Recommendations for Combined Aesthetic Interventions in the Face Using Botulinum Toxin, Fillers, and Energy-Based Devices. Dermatol Surg. 2016 May; 42(5): 586–97. doi: 10.1097/DSS.0000000000000754. PMID: 27100962.
[5] Carruthers J.D.A., Glogau R.G., Blitzer A. Facial Aesthetics Consensus Group Faculty. Advances in facial rejuvenation: botulinum toxin type a, hyaluronic acid dermal fillers, and combination therapies consensus recommendations. Plast Reconstr Surg. 2008 May; 121(5 Suppl): 5S-30S. doi: 10.1097/PRS.0b013e31816de8d0. PMID: 18449026.
[6] Chen S.Y., Lin J.Y., Lin C.Y. Vacuum-assisted Hydration before the Back-and-forth: A Novel Accelerating Method for Reconstituting Injectable Poly-D,L-lactic Acid. Plast Reconstr Surg Glob Open. 2021 May 13; 9(5): e3563. doi:10.1097/GOX.0000000000003563. PMID: 34881141; PMCID: PMC8647888.
[7] Cotofana S., Fratila A.A.M., Schenck T.L., Redka-Swoboda W., Zilinsky I. Pavicic Т. The Anatomy of the Aging Face: A Review. Facial Plast Surg. 2016 Jun; 32(3): 253–60. doi: 10.1055/s-0036–1582234. Epub 2016 Jun 1. PMID:27248022.
[8] https://www.cmjournal.ru/blogs/mezhdunarodnye-publikatsii-i-novosti/rossiyskiy-konsensus-ekspertov-po-primeneniyu-implantata-skulptra-poli-l-molochnaya-kislota-v-esteticheskoy-meditsine
[9] https://www.isaps.org/wp-content/uploads/2022/01/ISAPS-Global-Survey_2020.pdf
[10] Infante V.H.P., Bagatin E., Maia Campos PMBG. Skin photoaging in young men: A clinical study by skin imaging techniques. Int J Cosmet Sci. 2021 Jun;43(3):341–351. doi: 10.1111/ics.12701. Epub 2021 Apr 21. PMID: 33728691.
[11] Kapoor K.M., Chatrath V., Anand C., Shetty R., Chhabra C., Singh K., Vedamurthy M., Pai J., Sthalekar B., Sheth R. Consensus Recommendations for Treatment Strategies in Indians Using Botulinum Toxin and Hyaluronic Acid Fillers. Plast Reconstr Surg Glob Open. 2017 Dec 28; 5(12): e1574. doi:10.1097/GOX.0000000000001574. PMID: 29632761; PMCID:PMC5889450.
[12] Li G., Zhao M., Xu F., Yang B., Li X., Meng X., Teng L., Sun F., Li Y.Synthesis and Biological Application of Polylactic Acid. Molecules. 2020 Oct 29; 25(21): 5023. doi: 10.3390/molecules25215023.PMID: 33138232; PMCID: PMC7662581.
[13] Moers-Carpi M., Christen M.O., Delmar H., Brun P., Bodokh I.,Kestemont P. European Multicenter Prospective Study Evaluating Long-Term Safety and Efficacy of the Polycaprolactone-Based Dermal Filler in Nasolabial Fold Correction. Dermatol Surg. 2021 Jul 1;47(7):960–965. doi: 10.1097/DSS.0000000000002978. PMID: 33731572.
[14] Palm M., Weinkle S., Cho Y., LaTowsky B., Prather H. A Randomized Study on PLLA Using Higher Dilution Volume and Immediate Use Following Reconstitution. J Drugs Dermatol. 2021 Jul 1; 20(7): 760–766. doi: 10.36849/JDD.6034. PMID: 34232000.
[15] Rezaee Khiabanloo S., Nabie R., Aalipour E. Effectiveness of jawline, jaw angle, and marionette lines correction in combination with double needles threads (APTOS) and a collagen-stimulating dermal filler (ELLANSE): An innovative technique. J Cosmet Dermatol. 2022 May 4. doi: 10.1111/jocd.15042. Epub ahead of print. PMID: 35506203.
[16] Shao Y., Qin Z., Alexander Wilks J., Balimunkwe R.M., Fisher G.J., Voorhees J.J., Quan T. Physical properties of the photodamaged human skin dermis: Rougher collagen surface and stiffer/ harder mechanical properties. Exp Dermatol. 2019 Aug; 28(8):914–921. doi: 10.1111/exd.13728. Epub 2018 Jul 29. PMID:29957839; PMCID: PMC6311145.
[17] Shin J.W., Kwon S.H., Choi J.Y., Na J.I., Huh C.H., Choi H.R., Park K.C. Molecular Mechanisms of Dermal Aging and Antiaging Approaches. Int. J. Mol. Sci. 2019, 20, 2126.
[18] Singhvi M.S., Zinjarde S.S., Gokhale D.V. Polylactic acid: synthesis and biomedical applications. J Appl Microbiol. 2019 Dec; 127(6): 1612–1626. doi: 10.1111/jam.14290. Epub 2019 Jun 17. PMID: 31021482.
[19] Sundaram H., Signorini M., Liew S., Trindade de Almeida A.R., Wu Y., Vieira Braz A., Fagien S., Goodman G.J., Monheit G., Raspaldo H. Global Aesthetics Consensus Group. Global Aesthetics Consensus: Botulinum Toxin Type A-Evidence-Based Review, Emerging Concepts, and Consensus Recommendations for Aesthetic Use, Including Updates on Complications. Plast Reconstr Surg. 2016 Mar; 137(3): 518e-529e. doi: 10.1097/01.prs.0000475758.63709.23.
PMID: 26910696; PMCID: PMC5242214.
[20] Wu W.T.L., Liew S., Chan H.H., Ho W.W.S., Supapannachart N., Lee H.K., Prasetyo A., Yu J.N., Rogers J.D. Asian Facial Aesthetics Expert Consensus Group. Consensus on Current Injectable Treatment Strategies in the Asian Face. Aesthetic Plast Surg. 2020 Aug; 44(4): 1195–1207. doi: 10.1007/s00266-020–01818-8. Epub 2016 Feb 18. PMID: 32844269.
[21] Yutskovskaya Y.A., Sergeeva A.D., Kogan E.A. Combination of Calcium Hydroxylapatite Diluted With Normal Saline and Microfocused Ultrasound With Visualization for Skin Tightening. J Drugs Dermatol. 2020 Apr 1; 19(4): 405–411. doi: 10.36849/JDD.2020.4625. PMID: 32272518.

