
Илешина Т.В., кандидат медицинских наук, дерматовенеролог, косметолог, доцент кафедры дерматовенерологии ФГОУ ДПО ИПК ФМБА, главный врач СК «Вероника» (Москва)
Чайковская Е.А., кандидат фармацевтических наук, редактор ИД «Косметика и медицина» (Москва)
Попова О.П., кандидат биологических наук, зав. отделом клеточной и молекулярной патологии НИИ молекулярной медицины Первого MIMY им. И.М. Сеченова (Москва)
Возможность малоинвазивной коррекции локальных жировых отложений давно привлекает внимание исследователей, врачей и пациентов. В этом ракурсе мы говорим о процедурах лазерного, ультразвукового и криолиполиза, а также о некоторых инъекционных методах.
Инъекционный липолиз — именно так часто называют процедуры, направлен- ные на редукцию жировой ткани с помощью инъекционного введения соединений, тем или иным образом локально воздействующих на жировую ткань или жировой обмен. Достаточно часто в российских публикациях встречается упоминание «прямых липолитиков», к которым относят фосфатидилхолин (ФХ) и дезоксихолат натрия (ДХ), а также «непрямых липолитиков» — соединений, влияющих на процессы липолиза и липогенеза, на выведение и утилизацию продуктов гидролиза триглицеридов. К этой группе относят аминофиллин, теофиллин, кофеин, изопротеренол, карнитин, пируват кальция, йохимбин, экс- тракт артишока и др. [1-3].
На наш взгляд, многие из употребляемых сегодня терминовне совсем корректны. Природные детергенты, к которым относится ДХ (а он часто использует- ся в комбинации с OX), практически не влияют на обмен триглицеридов. По аналогии с другими деструктивными методами (лазерное, ультразвуковое или низкотемпературное воздействие) их введение в жировую ткань сопровождается разрушением адипоцитов (адипоцитолизом), высвобождением триглицеридов, которые включаются в естественный катаболизм и выводятся из области воздействия. Впервые термин «инъекционный адипоцитолиз» в клиническую практику ввел П. Мотолезе. В своих статьях он пишет о необхо- димости пересмотреть терминологию, описывающую процедуры коррекции контуров тела [4, 5]. Ведь липолиз — это естественный гормонозависимый метаболический процесс в адипоцитах. Если говорить о стимуляции процесса липолиза в интактной жировой ткани (прерогатива мезотерапии), то термин «инъекционный липолиз» логически обоснован, и можно обсуждать и изучать препараты с липолитическим действием (прямым или опосредованным — это уже второй вопрос). Но называть этим же термином метод, связанный с деструкцией клеток, по меньшей мере парадоксально. Термин «инъекционный адипоцитолиз» видится нам более оправданным с точки зрения характера воздействия, оказываемого на жировую ткань. Терминологическое обособ-ление методов инъекционного адипоцитолиза и инъекционного липолиза, возможно, будет способствовать более взвешенному отношению врачей к их применению, а также станет основой для размышлений о целесообразности сочетания различных препаратов — детергентов и липолитиков — в рамках одной процедуры.
Итак, инъекционный адипоцитолиз подразумевает локальную деструкцию под-кожной клетчатки, разрушение жировых клеток в зоне введения препарата на основе природных детергентов — ФХ и ДХ.
Фосфатидилхолин — собирательный термин для целой группы родственных соединений из класса фосфолипидов. В их состав кроме глицерина и жирных кислот входят фосфорная кислота и холин. Для ФХ организма человека харак- терно присутствие насыщенных жирных кислот — пальмитиновой, стеариновой и олеиновой. Для фармацевтических целей ФХ (лецитин) выделяют из соевых бобов. В его состав входят преимущественно ненасыщенные жирные кислоты — линолевая и а-линоленовая.
К подтвержденным биологическим эффектам ФХ относят его мембранопротекторное действие, участие в реализации целого ряда сигнальных путей, проведении нервного импульса. Фосфатидилхолин выполняет роль сурфактанта вальвеолах легких, ингибирует агрегацию тромбоцитов. В составе липопротеинов участвует в транспорте холестерина; эмульгируя триглицериды, делает их более доступными для триглицеридлипазы. Показания к применению инъек- ционного препарата ФХ — липостабила — профилактика и лечение жировой эмболии, гиперлипидемии, коронарного атеросклероза. Фармакология препарата связана с его эмульгирующим действием в отношении липидов эмбола или атеросклеротической бляшки.
Что касается жировой ткани, то в исследованиях последних лет показано, что в культуре адипоцитов ФХ не стимулирует процесс липолиза [5, 6], однако способствует перераспределению липидов с уменьшением их количества внутри клеток и повышением уровня внеклеточных липидов [7]. В концентрации менее 1 мг/мл ФХ не проявляет цитотоксичность по отношению к фибробластам, но активизирует апоптоз преадипоцитов посредством фосфорилирования протеинов стрессового сигнального пути и активизации каспаз 3, 8 и Этипов [8].
Для нас интересен следующий факт, обнаруженный в экспериментах in vitro: при использовании комплексного препарата, включающего помимо ФХ дезоксихо- лат натрия, теряются особые свойства ФХ, как то способность активизировать апоптоз адипоцитов [9]. И на первый план выходят биологические эффекты ФХ.
В сравнительных клинических исследованиях Rotunda, Salti, Duncan [9, 10, 11] показали, что эффект редукции жировой ткани после введения ФХ/ДХ и толь- ко ДХ практически одинаков, исходя из чего авторы сделали вывод о ведущей роли ДХ в этой композиции для инъекционного адипоцитолиза. В целом ряде клинических исследований изучается действие монопрепаратов на основе ДХ [10, 12, 13]. Почему же так часто речь идет еще и о OX?
Дело в том, что OX нерастворим в воде, и для создания его инъекционной формы на водной основе необходим эмульгатор. В этой роли в большинстве лекар- ственных форм OX используется именно ДХ (рис. 1).
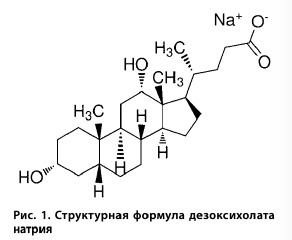
Дезоксихолевая кислота относится к группе вторичных желчных кислот, кото- рые синтезируются микрофлорой толстого кишечника из первичных желчных кислот, например холевой, которая, в свою очередь, образуется в печени из холестерина. 90-95% дезоксихолевой кислоты реабсорбируется в кишечнике и поступает в кровь, а затем вновь секретируется печенью в просвет кишечника в составе желчи. Около 1 г ДХ постоянно задействовано в гепатоэнтеральной циркуляции. Концентрация ДХ в периферической крови составляет приблизительно 0,56 ммоль/л.
Поскольку ДХ в составе различных препаратов ФХ долгое время считался вспомогательным компонентом (эмульгатором), его собственное биологиче- ское действие не рассматривалось, а все эффекты от введения препаратов в жировую ткань относили к OX. Теперь наши представления кардинально изменились.
При введении в культуру адипоцитов ДХ вызывает лизис клеток, для OX такой эффект не обнаружен [6] (рис. 2).

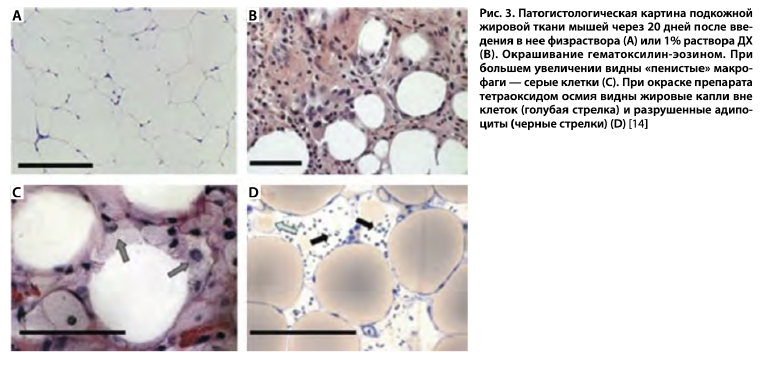
Экспериментальное исследование на мышах показало, что введение ДХ в подкожную жировую ткань (трехкратные инъекции по 200 мкл 1% раствора ДХ) сопровождается деструкцией адипоцитов и иммунным ответом в виде развития воспалительного инфильтрата с привлечением гистиоцитов, которые на патогистологических препаратах при большом увеличении видны как «пенистые» клетки [14] (рис. 3). Важно отметить, что на фоне выраженных изменений в жировой ткани кожа и мышцы остаются достаточно сохранными, без признаков некроза и с минимальной выраженностью воспалительной инфильтрации.
Тем не менее, исследования на культуре тканей показали цитотоксичность ДХ в отношении различных клеток: концентрация ДХ, при которой погибает 50% клеток, для адипоцитов составляет 0,045%; для фибробластов и миоцитов — 0,055%; для кератиноцитов — 0,015% [14]. По данным Gupta и соавт., максимальной чувствительностью к ДХ обладают миоциты и клетки эндотелия сосудов [7]. Причем оказывается, что в культуре клетки разных типов оказываются гораздо более чувствительными к действию ДХ, чем в условиях т vivo. Почему? Дело в том, что ДХ обладает высокой аффинностью к альбумину и, связываясь с ним, теряет способность разрушать клеточные мембраны. Альбумин всегда присутствует во внеклеточном матриксе как жировой ткани, так и дермы, и мышечной ткани. Причем в дерме и мышечной ткани концентрация альбумина выше, чем в жировой. Вероятно, именно этим объясняется более слабое повреждение клеток кожи и мышц под действием ДХ. Равно как и сохранение целостности стенки кишечника и кровеносных сосудов на фоне достаточно высокого уровня ДХ: именно в этих тканях уровень альбумина очень высок [15]. Еще раз подчеркнем неспецифическое цитолитическое действие ДХ в отношении всех типов исследованных клеток, что является клиническим посылом для прецизионно точного проведения инъекций препаратов с ДХ именно в жировую ткань, при- чем в областях, где она имеет достаточную толщину. В противном случае мы наблюдаем осложнения в виде стойкого воспалительного процесса в коже и даже некрозов [16].
Что мы наблюдаем в клинических условиях? По данным Уадита Одо и соавт. [17], при введении в подкожную жировую клетчатку растворов ДХ в местах инъекций немедленно развивается дозозависимый лизис адипоцитов в рамках некроза жировой ткани. Процесс сопровождается лимфомононуклеарной инфильтрацией, активным фагоцитозом фрагментов разрушенных клеток и жи-ровых капель макрофагами. Спустя 6 мес после инъекций обнаруживаются яв- ления фиброзирования.
На первом этапе клинических испытаний препарата АТХ-101 (KYTHERA Biopharmaceuticals, США) было установлено, что в отличие от плацебо ДХ приводит к выраженной деструкции адипоцитов в месте инъекции с локальным иммунным ответом и утолщением фиброзных септ в жировой ткани [18].
По данным Эль Камшоуши и соавт. в клинических условиях через 2 нед после инъекций ДХ (Deoxylase, Aesthetic Dermal, Испания. Концентрация ДХ 25 мг/мл., вводили 8 мл препарата) в подкожную жировую ткань абдоминальной области на патогистологических препаратах помимо некроза с явлениями фиброза в жировой ткани наблюдается выраженный некробиоз нижних слоев дермы, фиброз в области придатков кожи (волосяных фолликулов и потовых желез) и их атрофия [19].
Аналогичными наблюдениями делятся Schuuller-Petrovic и соавт. [20]: в эксперименте на крысах и в клинических условиях после введения ФХ/ДХ или только ДХ в жировую ткань исследователи наблюдали дозозависимый цитотоксический эффект в отношении адипоцитов, некроз жировой ткани, фиброплазию в областях соприкосновения с мышцами, формирование кист и некротические изменения в области тонких кровеносных сосудов. Авторы высказывают озабоченность относительно безопасности процедур инъекционного адипоцитолиза.
Однако накопленный к сегодняшнему дню клинический опыт, разработка особых видов техники инъекций биодетергентов и наличие препаратов научно обоснованного состава позволяют говорить о безопасности и эффективности метода инъекционного адипоцитолиза [21].
Препарат Акваликс (Ghimas Spa, Италия), известный также как раствор Moтолезе, представляет собой водный раствор дезоксихолата натрия (8%), равномерно распределенного в гелевой среде полигалактозы. Использова- ние вязкой буферной среды обеспечивает пролонгированное высвобождение ДХ, что ограничивает распространение раствора и диффузию препарата, т.е. способствует локализации его цитолитического действия. Все это позволяет проводить безопасные процедуры локальной редукции поверхностной жировой ткани.
Акваликс имеет сертификат ЕС и, начиная с 2009 г. широко применяется в 50 странах, включая Россию. Показания к применению: коррекция локальных жировых отложений, гиперплазии подкожной жировой ткани в отдельных областях, «бычьего горба» у пациентов со СПИД.
Мотолезе была разработана и особая техника введения препарата, подразумевающая использование игл (канюль) длиной 10-15 см для проведения линейных инъекций препарата в проблемной зоне [21]. По опыту работы российских специалистов, инъекции Акваликса следует выполнять с помощью игл длиной 7и10см [22]. Инъекции проводятся по векторам, расположенным параллельно поверхности кожи, обычно в виде веера. Таким образом обеспечивается максимальное насыщение детергентом жировой ткани и ограничивается его воздействие на кожу и подлежащие мышцы. В отличие от традиционной техники вертикальных вколов при проведении линейных инъекций уменьшается риск формирования фиброзных узловых образований [16, 21]. Методика, объединяющая использование препарата Акваликс и проведение линейных инъекций, названа Мотолезе «интралипотерапией».
В нашей стране активно накапливается и обобщается опыт работы с Акваликсом [16, 22, 23]. При соблюдении всех необходимых условий — наличие показаний к проведению процедуры, использование небольших объемов препарата, поэтапное проведение коррекции с применением адекватной техники — достигаются убедительные результаты при невысоком уровне нежелательных явлений.
Основной жалобой пациентов являются жжение, болезненность, покраснение и уплотнение области инъекций, появление точечных и мелкоочаговых кровоизлияний сразу после процедуры. Для уточнения природы наблюдаемой клинической картины, а также механизма действия ДХ в составе препарата Акваликс нами было проведено изучение патогистологической картины в биоптатах жировой ткани, полученных через 30 мин после введения препарата в жировую ткань абдоминальной области добровольцев.
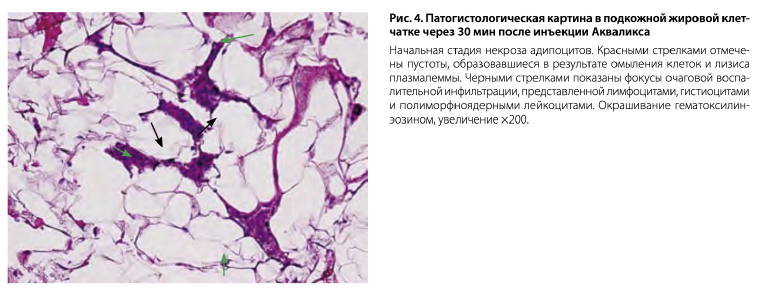
На патогистологических препаратах подкожная жировая клетчатка пред- ставлена относительно крупными мономорфными клетками (адипоцитами) сферической (округлой и овальной) формы, с оптически пустой цитоплазмой, окруженными тонкой сеткой ретикулярных волокон с немногочисленными капиллярами (рис. 4). Наблюдаются участки, представленные несколько сжатыми, деформированными полигональными адипоцитами, расположенными вблизи фокусов разрушения клеток (некроза), в которых отмечается нарушение целостности клеточных мембран с образованием пустот и крупных аморфных жировых вакуолей. Перифокальная очаговая воспалительная инфильтрация представлена лимфоцитами, гистиоцитами и полиморфноядерными лейкоцитами, присутствие которых манифестирует начало острой фазы воспаления. Таким образом, механизм действия ДХ в составе препарата Акваликс связан с некрозом жировой ткани на фоне лизиса адипоцитов, развитием характерной посттравматической воспалительной реакции. Фиброзирование жировой ткани, наблюдаемое после инъекционного адипоцитолиза и неоднократно описанное в литературе, формируется в более поздние сроки (от 2 нед до нескольких месяцев после проведения инъекций) и представляет собой исход некротического процесса. Воспалительный процесс на уровне кожи является, скорее всего, опосредованным и обусловлен массовой секрецией провоспа- лительных цитокинов иммунокомпетентными клетками в зоне адипоцитолиза. Кровоизлияния, возможно, связаны с некротическим повреждением стенки кровеносных сосудов.
Обсуждение
На сегодняшний день мы имеем два инъекционных метода коррекции объема жировой ткани:
- инъекционный липолиз (мезотерапия), подразумевающий активизацию липолитических и дренажных процессов в жировой ткани без повреждения адипоцитов;
- инъекционный адипоцитолиз с использованием препаратов ДХ, разрушающих адипоциты C последующим удалением фрагментов клеток и триглицеридов в ходе некротического процесса.
Принципиальные различия механизма действия препаратов в рамках двух методов ставят под сомнение целесообразность их комбинирования в одной лекарственной форме. Хотя можно привести немало примеров препаратов, включающих наряду с ФХ и ДХ еще и карнитин, инсулиноподобный фактор роста | типа, экстракт арники, комплексы витаминов, аминокислот, антиоксидантов. Насколько успешно реализуется биологическая активность этих соединений в условиях некроза жировой ткани — большой вопрос [2, 3]. Нередко звучит аргумент, что в случае применения комбинированных препаратов повышается комфортность процедуры, а также уменьшается степень выраженности нежелательных явлений после процедуры, риск формирования узловых образований. Но это связано, скорее всего, с тем, что менее агрессивно протекает процесс адипоцитолиза. Того же самого можно достичь при использовании разведенных препаратов ДХ или введении их в меньшем объеме.
Формирование клинического эффекта после проведения инъекционного адипоцитолиза (интралипотерапии) в виде сокращения жировых отложений и некоторой ретракции кожи можно объяснить процессами разрушения адипо- цитов, последующего дебридмента, а также фиброплазией в коже над местом инъекций. Эти процессы развиваются на протяжении 8-10 нед после инъекции/ курса инъекций [11, 24, 25]. Оставшиеся адипоциты существенно уменьшаются в размерах, что является косвенным свидетельством повышенного транспорта триглицеридов из жировых клеток [26].
Безопасными признаны инъекции в областях с достаточным слоем подкожной жировой ткани, к которым относятся абдоминальная область, боковые поверхности туловища, области над коленом и сбоку от него, переднебоковые поверхности бедер, а также субментальная зона с выраженным слоем надплатизмальной жировой клетчатки. Отдельно рассматриваются вопросы безопасной коррекции липом [12]. Специалисты делятся своим опытом успешной коррекции различных областей лица, однако такие инъекции нельзя признать безопасными, поскольку в настоящее время у нас нет отработанных протоколов и оттитрованных доз препарата.
Еще одно опасение относительно безопасности процедур инъекционного липолиза с точки зрения системных эффектов также снято с повестки дня: в клинических исследованиях показано, что после проведения инъекций ДХ или комбинации ФХ/ДХ уровень липидов и липопротеинов в крови несколько повышается, но находится в границах нормы [17, 26, 27]. Аналогичная тенденция наблюдается в отношении уровня глюкозы и инсулина, провоспалительных цитокинов, С-реактивного белка, печеночных трансфераз, амилазы. Уровень ДХ в крови также существенно не повышается [18].
Таким образом, методика интралипотерапии с применением ДХ (препарата Акваликс) в руках опытного врача является эффективным инструментом коррекции объема жировой ткани.
Литература
1. Rotunda A.M., Kolodney M.S. Mesotherapy and phosphatidylcholine injections: historical clarification and review. Dermatol Surg. 2006; 32 (4): 465—480.
2. Ширшакова М А. Мезотерапевтическая коррекция эдематозно- фиброзной панникулопатии (целлюлита) и локальных жировых отложений. ПХиК. 2010; 3: 445—449.
3. Ширшакова М А. Мезотерапия целлюлита: некоторые практические рекомендации, Инъекционные методы в косметологии. 2011; 2: 26-29.
4. Motolese P The medical language in aesthetic sciences, Eur J Aesth Med Dermatol. 2012; 2 (1): 6-7.
5. Motolese P Phospholipids do not have lipolytic activity. A critical review. J Cosmet Laser Ther. 2008; 10: 114-118.
6. Klein S.M., SchremI S., Nerlich M., Prantl L. In Vitro Studies Investigating the Effect of Subcutaneous Phosphatidylcholine Injections in the 313-L1 Adipocyte Model: Lipolysis or Lipid Dissolution? Plast Reconstr Surg. 2009; 124 (2):419-427,
7. Gupta А, Lobocki C, Singh S., Robertson M., Akadiri 0.4., Malhotra G., Jackson I.T. Actions and comparative efficacy of phosphatidylcholine formulation and isolated sodium deoxycholate for different cell types. Aesthetic Plast Surg. 2009; 33 (3): 346-352.
8. Li H., Lee J.H,, Kim S.¥. et al. Phosphatidylcholine induces apoptosis of 373-L1 adipocytes. J Biomed ба. 2011; 18:91.
9. Duncan D.L., Palmer М. Fat reduction using phosphatidytcholine/sodium deoxycholate injections: standard of practice. Aesthetic Plast Surg. 2008; 32 (6): 858-872.
10. Salti G.G, TantussiF, Bovani B,, Lotti. Phosphatidylcholine and sodium deoxycholate in the treatment of localized fat: a doubleblind, rando- mized study. Dermatol Surg. 2008; 34: 60-66.
Duncan D., Rubin J.P, Golitz L., Badylak $., Kesel L. Refinement of technique in injection lipolysis based on scientific studies and clinical evaluation. Clin Plast Surg. 2009; 36 (2): 195-209.
12. Ротунда А.М, Аблон Г., Колодни М.С. Лечение липом подкожными инъекциями дезоксихолата. Инъекционные методы в косметологии. 2012; 4: 82-86.
13. Rotunda A., Suzuki H., Moy R.L., Kolodney M.S. Detergent effects of sodium deoxycholate are a major feature of an injectable phosphatidy!- choline formula used for localized fat dissolution. Dermatol Surg. 2004; 30 (7): 1001-1008.
14. Thuangtong R., Bentow JJ., Knopp К, Mahmood N.A., David N.E., Koladney M.S. Tissue-selective effects of injected deoxycholate. Dermatol Surg. 2010; 36 (6): 899-908.
15. Илешина ТВ. Интралипотерапия: что, где, когда и зачем? Инъекционные методы в косметологии. 2013; 1: 94-100.
16. Дункан Д., Ротунда А.М. Инъехционная терапия для локальной редукции жировой ткани: современный взгляд. Инъекционные методы в косметологии. 2012; 1:38—53.
17. Yagima Odo МЕ. Cuce [.С.,, Odo LM, Natrielli А. Action of sodium deoxycholate on subcutaneous human tissue: local and systemic effects. Dermatol Surg. 2007 (2): 178—188.
18. http://wwwsec.gov/Archives/edgar/ data/1436304/000104746912006126/a2208613zs-1.htm.
19. Эль Камшоуши A., Абель Максауд P, Махди Н. Сравнительное исследование эффективности инъекционной редукции жировой ткани C использованием комплекса фосфатидилхолин/дезокси- холат и дезоксихолата в качестве монотерапии. Инъекционные методы в косметологии. 2013; 4: 14—27.
20. Schuuller-Petrovic S., Wucart G., Neuhold N., Freisinger Е, Brunner Е Tissue— toxic effect of phosphatidylcholin/deoxycholat after subcutane- ous injection for fat dissolution in rats and human volonunter. Dermatol Surg. 2008; 34: 529-542.
21. SaltiG,, Rauso В. Comments on «Injection Lipolysis With Phosphatidy|- choline and Deoxycholate». Aesth Surg J. 2014; 34 (4):639- 640.
22. имошенко ЕВ. Коррекция локальных жировых отложений
методом интралипотерапии, Инъекционные методы в косметоло- гии. 2013; 4: 28—32.
23. Горбунов Г. Интралипотерапия в контексте эволюции инъекционного липолиза. Kosmetik international. 2012; 5: 72—74.
24. Duncan 0... Lipodissolve for Subcutaneous Fat Reduction and Skin Retraction. Aesthetic Surg. 2005; 25: 530-543.
25. Hasengschwandtner Е. Injection Lipolysis for Effective Reduction of Localized Fat in Place of Minor Surgical Lipoplasty. Aesthetic Surg J. 2006; 26 (2): 125-130.
26. Hasengschwandtner F. et al. Detailed Documentation of One Lipolysis Treatment: Blood Values, Histology, and Ultrasound Findings. Aesthetic Surg. 2007; 27 (2): 204—211.
27. Reeds ОМ, Mohammed В5., Klein S., Boswell С.В, Young V.L. Meta- bolic and structural effects of phosphatidylcholine and deoxycholate injections on subcutaneous fat: a randomized, controlled trial. Aesthet Surg J. 2013; 33 (3): 400-408.

